Ez a cikk a különleges 2020. májusi kiadásunk része. Töltse le a teljes kiadást itt.
Kapcsolat
Catinean A, Neag AM, Nita A, Buzea M, Buzoianu AD.bacilusspp. Spórák - ígéretes kezelési lehetőség az irritábilis bél szindrómában szenvedő betegek számára.Tápanyagok- 2019; 11 (9): 1968.
Célkitűzés
Ennek a tanulmánynak a célja az volt, hogy összehasonlítsa a rifaximint, majd egy táplálék- vagy alacsony erjeszthető oligoszacharidot, diszacharidot, monoszacharidot és poliol (FODMAP) étrendet, spóraba-alapú probiotikus (megaporebiotikus) terápiával, önmagában, székhelly nélkül.
Vázlat
Nem vak, prospektív, randomizált, ellenőrzött klinikai vizsgálat. A résztvevőket 3 csoportra véletlenszerűen randomizálták:
- G1, bei dem die Teilnehmer eine 10-tägige Kur mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Kur mit einem nutrazeutischen Inhaltsstoff Bifidobacterium longum W11, lösliche Ballaststoffe und Vitamine B1B2B6und B12.
- G2, bei dem die Teilnehmer einen 34-tägigen Kurs erhielten Bazillus spp probiotisch (Bacillus licheniformis, Bacillus indicus HU36™, Bacillus subtilis HU58™, Bacillus clausii, Bacillus coagulansalle von der Marke MegaSporeBiotic).
- G3, bei dem die Teilnehmer eine 10-tägige Behandlung mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Low-FODMAP-Diät.
A kutatók kiindulási intézkedéseket kaptak a kiindulási, 10. napon (G1 és G3 csoportok esetében), a 34. és a 60. napon.
Résztvevő
Ebben a tanulmányban 90 ingerlékeny bél szindrómában szenvedő beteg volt, székrekedés nélkül, a Róma III kritériumai alapján. A betegek 18 és 75 év közöttiek voltak, és az elmúlt öt évben normál kolonoszkópiával rendelkeztek, a vérértékek a referenciaértékekben és a normál széklet -kalprotektinben. Dokumentált élelmiszer -allergiában, glutén intoleranciában vagy celiakia, cukorbetegségben, pajzsmirigybetegségben, gyulladásos bélbetegségben vagy más szerves betegségek, étkezési rendellenességek (anorexia vagy bulimia), probiotikumok, probiotikumok, a vizsgálat előtt, az antibiotikumkezelés, az elmúlt 6 hónapban, vagy a specifikus étrendet kizárták.
A vizsgált vizsgálati paraméterek
A kutatók az IBS súlyossági pontszáma (IBS-SS), az IBS-betegek (IBS-QL) és a végbél térfogat-szenzációs teszt alapján értékelték a betegeket.
Kulcsfontosságú betekintés
Az IBS-SS javult minden G1, G2 és G3 eredménymérésnél, és érdekes módon a vizsgálat végéig is javult. A Megasporebiotikus csoport, a G2, a 3. látogatáskor (34. nap) korábbi tünetek javult. Az életminőségi pontszámok és a végbélmennyiség -szenzációs teszt szintén javult az egyes csoportokban, hasonló eredményekkel az egyes csoportokban.
Gyakorlati következmények
Az irritábilis bél szindróma egy gyakori rendellenesség, amely a populáció kb. 10% -át érinti, jelentős hiányosságokkal a megbízható és költséghatékony kezelési stratégiákban.1A patofiziológia megértése gyorsan növekszik a szisztémás biológia alkalmazásával. A jelenleg javasolt modell a bél mikrobiota diszfunkciójának, a megváltozott bélpermeabilitás, a megváltozott motilitás, a gyomor-bél (GI) immunsejtek aktiválása, a zsigeri túlérzékenység és a rendellenes bél-agy kölcsönhatások összetett hálója.2A Rifaximin először hatékony kezelési lehetőségként jelent meg a GI Microbiota 2011 -es megváltoztatásának a célkísérletével, amely végül a rifaximin FDA jóváhagyásához vezetett az IBS hasmenéssel történő kezelésére 2015 -ben.3Ennek a tanulmánynak a célja, hogy megmutassa, hogy a nem antibiotikus terápia a mikrobiome spóra-alapú probiotikummal történő megváltoztatásával szintén hatékony lehet az IBS hasmenés (IBS-D) kezelésére.
A tanulmány egyik legizgalmasabb aspektusa a spóra-alapú probiotikumok költséghatékonysága a rifaximinhez képest.
Ez a tanulmány számos jelentős korlátozást tartalmaz, amelyek közül sok a szerzők elismerik. Ide tartozik a vakítás és a placebo hiánya, a kiindulási állapotban a súlyos, nem pedig a súlyos tünetek, a vékonybél baktériumok túlnövekedésének (SIBO) légzésvizsgálatának hiánya, valamint a Róma III, nem pedig a Róma IV kritériumok felhasználása. A kutatók a Róma III -t használták, mert ez a tanulmány IV. Róma előtt kezdődött, és a szerzők megjegyzik, hogy a résztvevők 90% -a is teljesítette az új kritériumokat.
Vannak további korlátozások, amelyeket a szerzők nem tárgyalnak. Az első és talán a legfontosabb az, hogy a rifaximin -kezelési csoportot mind dózisban, mind időtartamban alulkezelték. A rifaximin jelenleg általánosan elfogadott adagolása az IBS-D-hez napi háromszor 550 mg (1650 mg teljes napi adag) 14 napig.4Ebben a tanulmányban napi 1200 mg -ot használtunk 10 napig, ami a tényleges dózis 52% -a. Ez jelentős eredmény-torzítást eredményez a spóra-alapú probiotikus beavatkozáshoz képest.
A továbbfejlesztett eredménymérések megerősíthetik ezt a tanulmányt. Először, a szerzők végbélmennyiség -szenzációs tesztet alkalmaztak a kiindulási és minden látogatáskor. Ez a teszt invazív, kényelmetlen, és az irodalomban kevés támogatást nyújt az IBS-D kimenetelének.5A végbél térfogat-szenzációs teszt helyett egy nem invazív 3 órás laktulóz-légzésvizsgálat javítaná a vizsgálat kialakítását. Ez lehetővé tette volna a szerzők számára, hogy csak SIBO -ban szenvedő betegeket vehetnek fel, vagy a SIBO státusza alapján az egyes kezelési csoportokban rétegezzék a válaszadókat. Rezaie et al. Megállapította, hogy a SIBO pozitív laktulóz-légzési tesztjében szenvedő betegek szignifikánsan jobban reagáltak a rifaximin-terápiára, mint az IBS-D-ben szenvedő betegek normál légzési teszttel.6A 3 órás laktulóz-légzésvizsgálat bevonása ebben a tanulmányban tisztázta volna, hogy mely betegek voltak a legjobb jelöltek spóra-alapú probiotikus kezelésre, szemben a rifaximin-kezeléssel.
2 kezelési csoport (rifaximin/alacsony FODMAP étrend és spóra-alapú probiotikus) vagy 2 kezelési csoport használata, és egy placebo csoport javította volna az eredmények egyértelműségét. A vakítás kiküszöbölheti az elfogultság másik forrását; A terápiás táplálkozást azonban lehetetlen a szokásos táplálkozáshoz vakítani, és ez a táplálkozási kutatás folyamatos kihívása.
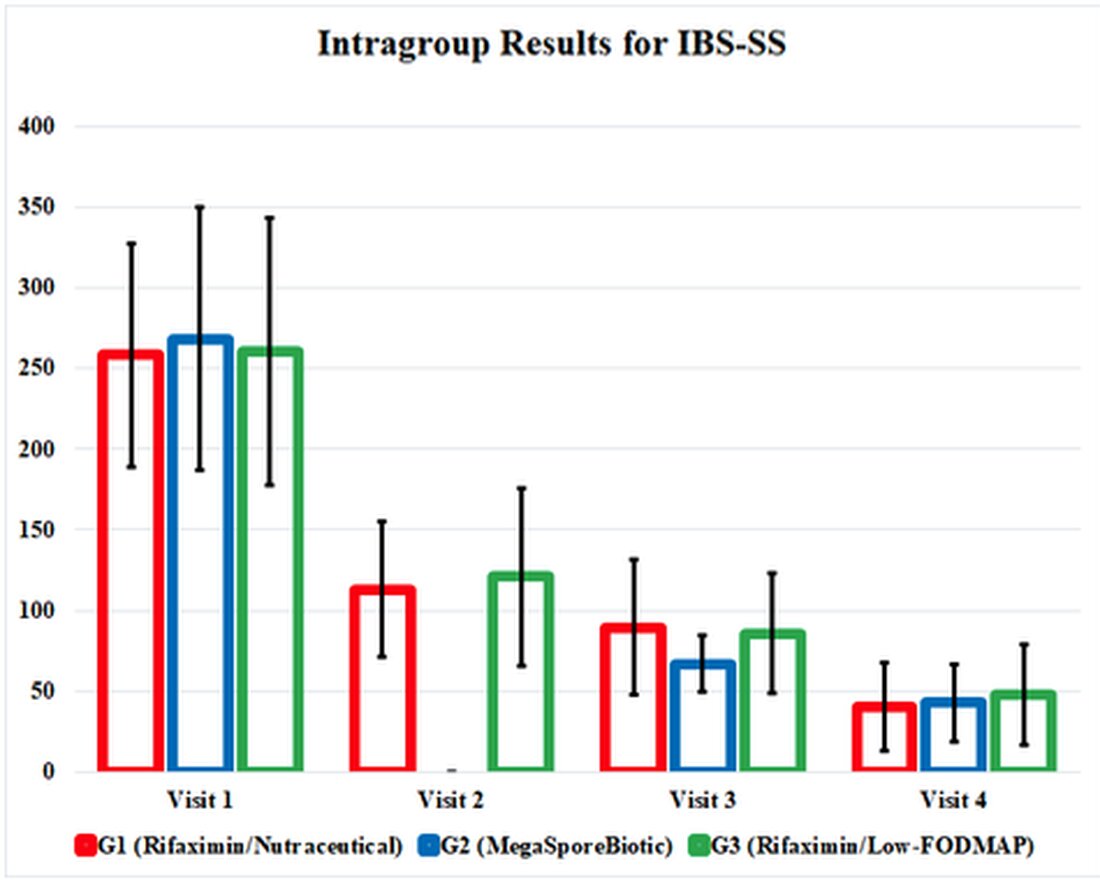
A tanulmányban a terápiás beavatkozások hatásait zavaró és nehézkes táblákba temették el, tehát a pozitív eredményeket kiemeltem egy grafikán, amely szemlélteti a tanulmány eredményeit. Ez a grafika bemutatja a tanulmány eredményeit, és megmutatja nekünk, mennyire hatékonyan hasonlítják össze ezeket a terápiákat egymással. Ez azt is kiemeli, hogy mindhárom kezelési csoport tovább javult, még akkor is, ha a beavatkozásokat a 3. látogatáskor megszüntették (34. nap).
A tanulmány egyik legizgalmasabb aspektusa a spóra-alapú probiotikumok költséghatékonysága a rifaximinhez képest. A tanulmányban felhasznált rifaximin -dózis körülbelül 1300 dollárba kerül, és az ajánlott adag közelebb áll a 2000 dollárhoz. A biztosítási fedezet gyakran több gyógyszeres kudarcot és korábbi engedélyeket igényel, ha a kezelést egyáltalán fedezik. Az ebben a tanulmányban használt spóra-alapú probiotikum dózisa és időtartama 55 dollárért árul. Ez a spóra-alapú probiotikus terápia jelentős előnyeit jelenti. A szerzők nem jelentettek mellékhatásokat vagy a résztvevők lemorzsolódását, ezért ezeket a tényezőket nehéz figyelembe venni a költséghatékonysági arányba.
Azt is meg kell jegyezni, hogy az eredmények hasonlóak voltak a spóra-alapú probiotikus terápiához, mint az alacsony FODMAP étrend-kezelési csoporthoz képest. Kimutatták, hogy az alacsony FODMAP-étrend hatékony táplálkozási stratégia az IBS-D kezelésére.7Noha izgalmas az IBS hatékony táplálkozási eszköze, ez az étrend nagyon korlátozó, és messzemenő pszichoszociális és táplálkozási hatással rendelkezik.8Tapasztalataim szerint az alacsony FODMAP étrend stresszesebb étrend, mint más, talán még szigorúbb étrend, mivel az ételek választása nem intuitív. A betegeknek folyamatosan kell használniuk az anyagokat és az alkalmazásokat, ezért nagyon ébernek kell lenniük, hogy sikeresen kövessék ezt az étrendet. Ebben a tekintetben a spóra-alapú probiotikus terápia jelentős előnyt jelent.
Következtetés
Noha ennek a tanulmánynak számos módszertani kérdése van, amelyek torzítják az elfogultságot, fontos felismerni, hogy a tanulmány eredményei javítják az IBS-D kezelési lehetőségeinek megértését. A spóra-alapú probiotikus terápia önálló terápiaként az IBS súlyosságának, életminőségének és végbélmeneti térfogat-szenzációjának javulásával jár a rifaximin-terápiával, amelyet alacsony FODMAP étrend vagy probiotikus terápia követ. A tünetek tovább javultak a kezelés abbahagyása után mind a három beavatkozásnál, amint azt a javított IBS súlyossági pontszámok igazolják a 60. napon, összehasonlítva a 34. napra a kezelés abbahagyása után. A vizsgálat legjelentősebb hibája a kezeléshez szükséges rifaximin nem volt elegendő adagja. Ennek ellenére a spóra-alapú probiotikus terápia sokkal egyszerűbb kezelést kínál a rifaximin költségeinek kevesebb, mint 5% -ánál. További kutatásokra van szükség, mielőtt a spóra-alapú probiotikus terápia ugyanolyan hatékony, mint a rifaximin, de az IBS-D betegek kezelési lehetőségeinek kiválasztásakor minden bizonnyal figyelembe lehet venni.

 Suche
Suche
 Mein Konto
Mein Konto