Tämä artikkeli on osa erityistä toukokuun 2020 numeroa. Lataa koko ongelma täältä.
Suhde
Cattinean A, Neag AM, Nita A, Buzea M, Buzoianu AD.basillispp. Itiöt - lupaava hoitovaihtoehto potilaille, joilla on ärtyvän suolen oireyhtymä.Ravintoaineet. 2019; 11 (9): 1968.
Tavoite
Tämän tutkimuksen tavoitteena oli verrata rifaksimiinia, jota seurasi ravitsemus- tai alhainen käymiskykyinen oligosakkaridi, disakkaridi, monosakkaridi ja polyol (FODMAP) -ruokavalio, jolla on itiöpohjainen probioottinen (megasparebioottinen) terapia yksin potilailla, joilla on huolittava suolen oireyhtymä (IBS) ilman uripaatiota.
Luonnos
Särkymätön, mahdollinen, satunnaistettu, kontrolloitu kliininen tutkimus. Osallistujat satunnaistettiin kolmeen ryhmään:
- G1, bei dem die Teilnehmer eine 10-tägige Kur mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Kur mit einem nutrazeutischen Inhaltsstoff Bifidobacterium longum W11, lösliche Ballaststoffe und Vitamine B1B2B6und B12.
- G2, bei dem die Teilnehmer einen 34-tägigen Kurs erhielten Bazillus spp probiotisch (Bacillus licheniformis, Bacillus indicus HU36™, Bacillus subtilis HU58™, Bacillus clausii, Bacillus coagulansalle von der Marke MegaSporeBiotic).
- G3, bei dem die Teilnehmer eine 10-tägige Behandlung mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Low-FODMAP-Diät.
Tutkijat saivat tulosmittauksia lähtötilanteessa, päivänä 10 (ryhmille G1 ja G3), päivä 34 ja 60.
Osallistuja
Tämä tutkimus sisälsi 90 potilasta, joilla oli ärtyvän suolen oireyhtymä ilman ummetusta Rooman III kriteerien perusteella. Potilaat olivat 18–75 -vuotiaita, ja heillä oli normaali kolonoskopia viimeisen viiden vuoden aikana, vertailuarvojen ja normaalin fekaalisen kalproteektiinin veriarvot. Potilaat, joilla on dokumentoituja ruoka -allergioita, gluteeni -intoleranssia tai keliakiaa, diabeteksen, kilpirauhasen sairauden, tulehduksellisen suolistosairauden tai muut orgaaniset sairaudet, syömishäiriöt (anoreksia tai bulimia), probiootit 1 kuukausi ennen tutkimusta, antibioottihoito viimeisen kuuden kuukauden aikana tai spesifiset ruokavaliot suljettiin.
Arvioitu tutkimusparametrit
Tutkijat arvioivat potilaita IBS-vakavuuspisteiden (IBS-SS), IBS-potilaiden (IBS-QL) elämänlaadun ja peräsuolen tilavuuden sensaatiokokeen perusteella.
Keskeiset oivallukset
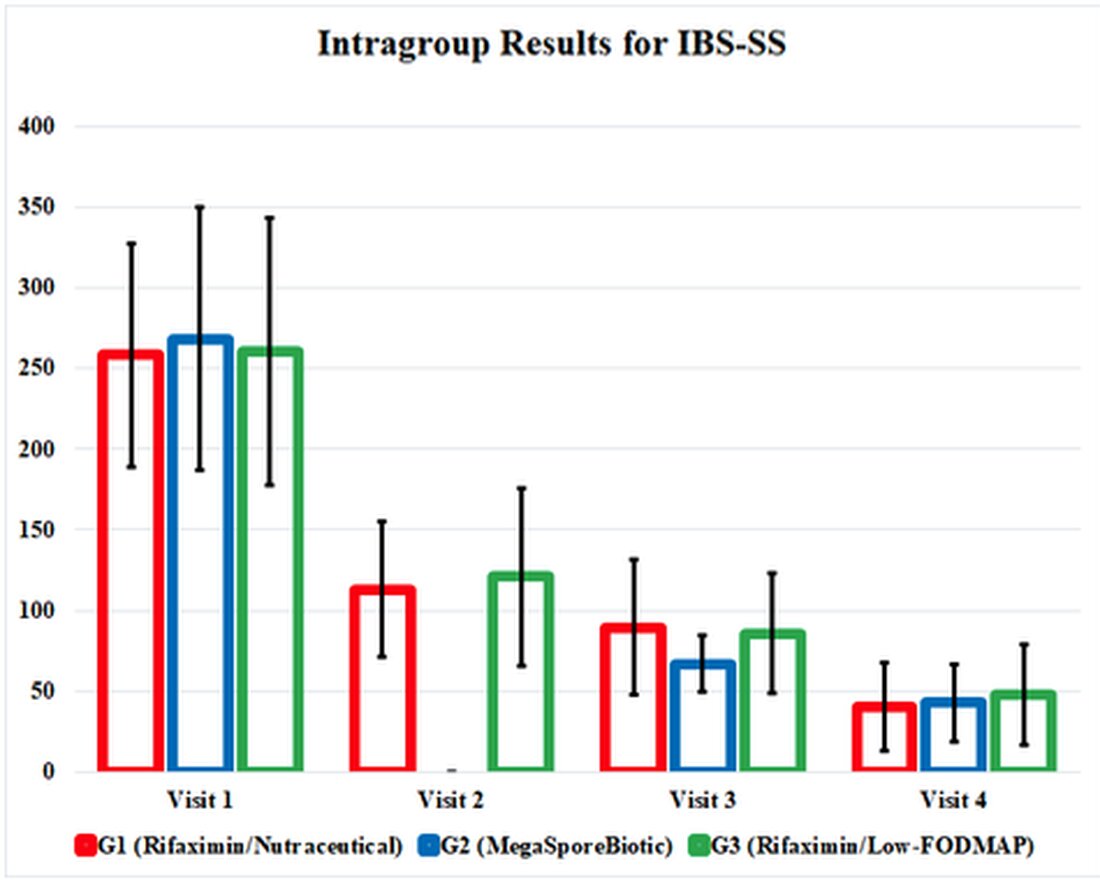
IBS-S: t paranivat jokaisessa G1: n, G2: n ja G3: n tulosmittauksessa ja mielenkiintoisesti parannettuna tasaisesti tutkimuksen loppuun mennessä. Megasporebiotiikkaryhmässä G2 oli aikaisemmin parannus vierailulla 3 (päivä 34). Elämänlaadun pisteet ja peräsuolen tilavuuden sensaatiotesti parani myös kussakin ryhmässä, ja samanlaiset tulokset kussakin ryhmässä.
Käytännöt
Ärsyttävän suoliston oireyhtymä on yleinen häiriö, joka vaikuttaa noin 10%: iin väestöstä, ja merkittävät aukot luotettavissa ja kustannustehokkaissa hoitostrategioissa.1Ymmärrysmme patofysiologiasta laajenee nopeasti systeemisen biologian avulla. Tällä hetkellä ehdotettu malli on monimutkainen suoliston mikrobiotan toimintahäiriö, muuttunut suoliston läpäisevyys, muuttunut liikkuvuus, maha-suolikanavan (GI) immuunisolujen aktivointi, viskeraalinen yliherkkyys ja epänormaali suolisto-aivo-vuorovaikutus.2Rifaksimiini nousi ensin tehokkaana hoitovaihtoehtona GI -mikrobiotan muuttamiseksi vuonna 2011 kohdetutkimuksella, mikä lopulta johti Rifaximinin FDA: n hyväksymiseen IBS: n käsittelyyn ripulilla vuonna 2015.3Tämän tutkimuksen tarkoituksena on osoittaa, että ei-antibioottihoito muuttamalla mikrobiomia itiöpohjaisella probiotilla voi myös olla tehokas IBS: n hoitoon ripulilla (IBS-D).
Yksi tämän tutkimuksen mielenkiintoisimmista näkökohdista on itiöpohjaisten probioottien kustannustehokkuus verrattuna rifaksimiiniin.
Tämä tutkimus sisältää useita merkittäviä rajoituksia, joista monet kirjoittajat tunnustavat. Näihin kuuluvat sokean ja lumelääkkeen puute, kohtalaiset kuin vakavat oireet lähtötilanteessa, pienen suolen bakteerien ylikuorman (SIBO) hengitystestauksen puute ja Rooman III käytön eikä Rooman IV kriteerien käyttö. Tutkijat käyttivät Rooman III, koska tämä tutkimus alkoi ennen Roomaa IV, ja kirjoittajat huomauttavat, että 90% osallistujista täytti myös uudet kriteerit.
Kirjailijat eivät keskustele ylimääräisiä rajoituksia. Ensimmäinen ja ehkä tärkein on, että rifaksimiinihoitosryhmä oli alikaivotettu sekä annoksella että kestolla. Rifaksimiinin yleisesti hyväksytty annos IBS-D: lle on 550 mg 3 kertaa päivässä (1 650 mg päivittäistä annosta) 14 päivän ajan.4Tässä tutkimuksessa 10 päivän ajan käytettiin yhteensä 1200 mg päivässä, mikä on 52% tehokkaasta annoksesta. Tämä johtaa merkittävään tuloksen puolueellisuuteen verrattuna itiöpohjaiseen probioottiseen interventioon.
Parannetut tulosmittaukset voisivat vahvistaa tätä tutkimusta. Ensinnäkin kirjoittajat käyttivät peräsuolen tilavuuden sensaatiotestiä lähtötilanteessa ja jokaisessa vierailussa. Tämä testi on invasiivinen, hankala ja sillä ei ole juurikaan tukea kirjallisuudessa IBS-D: n lopputuloksena.5Peräsuolen tilavuuden tunne-testin sijasta ei-invasiivinen 3-tunnin laktulosan hengitystesti parantaisi tutkimuksen suunnittelua. Tämä olisi antanut kirjoittajille mahdollisuuden sisällyttää vain SIBO -potilaat tai stratifioida vastaajat jokaisessa hoitoryhmässä SIBO -tilan perusteella. Rezaie et ai. havaitsi, että potilaat, joilla oli positiivinen laktulosan hengitystesti SIBO: lle, reagoivat merkittävästi paremmin rifaksimiinihoitoon kuin IBS-D-potilaat, joilla oli normaali hengitystesti.6Kolmen tunnin laktulosan hengitystestin sisällyttäminen tässä tutkimuksessa olisi selventänyt, mitkä potilaat olivat parhaita ehdokkaita itiöpohjaiseen probioottihoitoon verrattuna rifaksimiinihoitoon.
Kahden hoitoryhmän (rifaksimiini/matala-fodmap-ruokavalion verrattuna itiöpohjaiseen probioottiin) tai 2 hoitoryhmän käyttöä ja lumelääkeryhmä olisi parantanut tulosten selkeyttä. Sokeuttaminen voisi poistaa toisen puolueellisuuden lähteen; Terapeuttista ravitsemusta on kuitenkin mahdotonta sokea tavanomaiseen ravitsemukseen, ja tämä on jatkuva haaste ravitsemustutkimuksessa.
Terapeuttisten interventioiden vaikutukset tässä tutkimuksessa haudattiin hämmentäviin ja hankalaihin taulukoihin, joten olen korostanut positiivisia tuloksia graafiseen havainnollistamiseen tutkimuksen tuloksia. Tämä grafiikka esittelee tutkimuksen tulokset ja osoittaa meille, kuinka tehokkaita näitä hoitoja verrataan toisiinsa. Se korostaa myös sitä tosiasiaa, että kaikki kolme hoitoryhmää jatkoi paranemistaan, vaikka interventiot lopetettiin vierailulla 3 (päivä 34).
Yksi tämän tutkimuksen mielenkiintoisimmista näkökohdista on itiöpohjaisten probioottien kustannustehokkuus verrattuna rifaksimiiniin. Tässä tutkimuksessa käytetty rifaksimiiniannos maksaa noin 1 300 dollaria, ja suositeltu annos on lähempänä 2000 dollaria. Vakuutusturva vaatii usein useita lääkityshäiriöitä ja ennakkolupaa, jos hoitoa katetaan ollenkaan. Tässä tutkimuksessa käytetyn itiöpohjaisen probiootin annos ja kesto on 55 dollaria. Tämä edustaa merkittävää etua itiöpohjaisessa probioottihoidossa. Kirjoittajat eivät ilmoittaneet sivuvaikutuksia tai osallistujien keskeyttämistä, joten näitä tekijöitä on vaikea ottaa huomioon kustannustehokkuussuhde.
On myös huomattava, että tulokset olivat samanlaisia itiöpohjaisessa probioottihoidossa verrattuna matalan fodmap-ruokavalion hoitoryhmään. Matala-fodmap-ruokavalion on osoitettu olevan tehokas ravitsemusstrategia IBS-D: n hoidossa.7Vaikka ruokavalio on erittäin rajoittava tehokas ravitsemustyökalu IBS: lle, tämä ruokavalio on erittäin rajoittava ja sillä on kauaskantoisia psykososiaalisia ja ravitsemuksellisia vaikutuksia.8Kokemukseni mukaan matala FODMAP -ruokavalio on stressaavampi ruokavalio verrattuna muihin, ehkä vieläkin rajoittaviin ruokavalioihin, koska ruokavalinnat eivät ole intuitiivisia. Potilaiden on jatkuvasti käytettävä monisteita ja sovelluksia, ja siksi heidän on tullut erittäin valppaana noudattaakseen tätä ruokavaliota. Tältä osin itiöpohjainen probioottihoito tarjoaa merkittävän edun.
Johtopäätös
Vaikka tässä tutkimuksessa on useita metodologisia kysymyksiä, jotka esittelevät puolueellisuutta, on tärkeää tunnustaa, että tämän tutkimuksen tulokset parantavat ymmärrystämme IBS-D: n hoitovaihtoehdoista. Itiöpohjainen probioottihoito itsenäisenä terapiana liittyi IBS: n vakavuuden, elämänlaadun ja peräsuolen tilavuuden tunne, joka vastaa rifaksimiinihoidon, jota seuraa matala-fodmap-ruokavalio tai probioottihoito. Oireet paransivat edelleen kaikkia kolmea interventiota hoidon lopettamisen jälkeen, mikä käy ilmi parantuneista IBS -vakavuuspisteistä päivänä 60 verrattuna päivään 34 hoidon lopettamisen jälkeen. Merkittävin virhe tutkimuksessa oli rifaksimiinin riittämätön annos hoitoon. Siitä huolimatta itiöpohjainen probioottihoito tarjoaa paljon yksinkertaisemman hoidon alle 5 prosentilla rifaksimiinin kustannuksista. Lisää tutkimusta tarvitaan, ennen kuin itiöpohjainen probioottihoidot voidaan väittää olevan yhtä tehokas kuin rifaksimiini, mutta sitä voidaan varmasti harkita valittaessa IBS-D-potilaille hoitovaihtoehtoja.

 Suche
Suche
 Mein Konto
Mein Konto