See artikkel on osa meie erilisest mai 2020. aasta numbrist. Laadige täielik probleem alla siit.
Suhe
Catinean A, Neag AM, Nita A, Buzea M, Buzoianu AD.batsillusspp. Eosed - paljutõotav ravivõimalus ärritunud soole sündroomiga patsientidele.Toitained. 2019; 11 (9): 1968.
Eesmärk
Selle uuringu eesmärk oli võrrelda rifaksimiini, millele järgnes toitaine- või madala kääritatav oligosahhariidi, disahhariidi, monosahhariidi ja polüooli (FODMAP) dieeti eostepõhise probiootikumi (Megasporebiootilise) raviga üksi ainult ärrituva soolesündroomiga (IBS) patsientidel ilma kõlblumiseta.
Eelnõu
Pimestamata, perspektiivne, randomiseeritud, kontrollitud kliiniline uuring. Osalejad randomiseeriti 3 rühma:
- G1, bei dem die Teilnehmer eine 10-tägige Kur mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Kur mit einem nutrazeutischen Inhaltsstoff Bifidobacterium longum W11, lösliche Ballaststoffe und Vitamine B1B2B6und B12.
- G2, bei dem die Teilnehmer einen 34-tägigen Kurs erhielten Bazillus spp probiotisch (Bacillus licheniformis, Bacillus indicus HU36™, Bacillus subtilis HU58™, Bacillus clausii, Bacillus coagulansalle von der Marke MegaSporeBiotic).
- G3, bei dem die Teilnehmer eine 10-tägige Behandlung mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Low-FODMAP-Diät.
Teadlased said tulemusnäitajaid algtasemel 10. päeval (rühmade G1 ja G3 jaoks), 34. ja 60. päeval.
Osaleja
See uuring hõlmas 90 ärritunud soolesündroomi patsienti ilma kõhukinnisuseta, tuginedes Rooma III kriteeriumidele. Patsiendid olid vanuses 18–75 aastat ja viimase 5 aasta jooksul oli normaalne kolonoskoopia, vereväärtused võrdlusväärtuste ja normaalse fekaalse kalprotektiini piires. Patsiendid, kellel on dokumenteeritud toiduallergia, gluteenitalumatus või tsöliaakia, diabeet, kilpnäärmehaigus, põletikulised soolehaigus või muud orgaanilised haigused, söömishäired (anoreksia või buliimia), probiootikumid 1 kuu enne uuringut, viimase 6 kuu antibiootikumiravi või konkreetsed dieedid jäeti välja.
Hinnatud uuringuparameetrid
Teadlased hindasid patsiente IBS raskusastme (IBS-SS), IBS-i patsientide (IBS-QL) elukvaliteedi ja rektaalse mahu sensatsiooni testi põhjal.
Peamised teadmised
IBS-SS paranes iga G1, G2 ja G3 tulemusnäitaja osas ning huvitaval kombel paranes uuringu lõpuks võrdselt. Megasporebiootilisel rühmal G2 oli sümptomite varasem paranemine visiidil 3 (34. päev). Igas rühmas paranesid ka elukvaliteedi skoorid ja rektaalse mahu sensatsiooni test, igas rühmas sarnased tulemused.
Praktiseerimine
Ärritatud soole sündroom on tavaline häire, mis mõjutab umbes 10% elanikkonnast, milles on olulised lüngad usaldusväärsetes ja kulutõhusates ravistrateegiates.1Meie arusaam patofüsioloogiast laieneb kiiresti süsteemse bioloogia abil. Praegu pakutud mudel on soolestiku mikrobiota düsfunktsiooni keeruline veeb, muutunud soolestiku läbilaskvus, muudetud liikuvus, seedetrakti (GI) immuunrakkude aktiveerimine, vistseraalne ülitundlikkus ja ebanormaalsed soolestiku-aju interaktsioonid.2Rifaksimiin kujunes kõigepealt tõhusaks ravivõimaluseks GI mikrobiota muutmiseks 2011. aastal sihtkatsega, mis viis lõpuks FDA rifaksimiini heakskiiduni IBS -i raviks kõhulahtisusega 2015. aastal.3Selle uuringu eesmärk on näidata, et mitte-antibiootiline ravi, muutes mikrobiomi spooripõhise probiootikumiga, võib olla efektiivne ka IBS-i raviks kõhulahtisusega (IBS-D).
Selle uuringu üks põnevamaid aspekte on spooripõhiste probiootikumide kulutõhusus võrreldes rifaksimiiniga.
See uuring sisaldab mitmeid olulisi piiranguid, mida paljud autorid tunnistavad. Nende hulka kuulub pimestamise ja platseebo puudumine, algtasemel pigem mõõdukad kui rasked sümptomid, peensoole bakterite ülekasvu (SiBO) ja Rooma III, mitte Rooma IV kriteeriumide kasutamine. Teadlased kasutasid Rooma III, kuna see uuring algas enne Rooma IV ja autorid märgivad, et ka 90% osalejatest vastas uutele kriteeriumidele.
Autorid ei aruta täiendavaid piiranguid. Esimene ja võib -olla kõige olulisem on see, et rifaksimiini ravirühm oli nii annuse kui ka kestuse alal. IBS-D jaoks on rifaksimiini praegu üldiselt aktsepteeritud annus 550 mg 3 korda päevas (1650 mg päevas päevas) 14 päeva jooksul.4Selles uuringus kasutati 10 päeva jooksul kokku 1200 mg päevas, mis on 52% efektiivsest annusest. See põhjustab spooripõhise probiootilise sekkumisega võrreldes olulist tulemust.
Täiustatud tulemusnäitajad võivad seda uuringut tugevdada. Esiteks kasutasid autorid algtasemel ja igal visiidil rektaalse mahu sensatsioonitesti. See test on invasiivne, ebamugav ja sellel on kirjanduses vähe tuge IBS-D tulemusnäitajana.5Rektaalse helitugevuse sensatsioonitesti asemel parandaks uuringu kavandamist mitteinvasiivne 3-tunnine laktuloos-test. See oleks võimaldanud autoritel kaasata ainult SIBO -ga patsiente või kihistada igas ravirühmas reageerijaid SIBO staatuse põhjal. Rezaie jt. leidis, et SIBO positiivse laktuloosiõhu testiga patsiendid reageerisid rifaksimiinravile oluliselt paremini kui normaalse hingetõmbega IBS-D patsiendid.6Kolmetunnise laktuloosiõhutesti kaasamine sellesse uuringusse oleks selgitanud, millised patsiendid olid parimad spooripõhise probiootilise ravi kandidaadid võrreldes rifaksimiinraviga.
Kahe ravirühma (rifaksimiin/madala foDmap-dieet versus spooripõhine probiootikum) või 2 ravirühma kasutamist ja platseeborühma oleks tulemuste selgust parandanud. Pimestamine võib kõrvaldada veel ühe eelarvamuse allika; Kuid tavapärase toitumise terapeutilist toitumist on võimatu pimedaks ja see on toitumisuuringute jätkuv väljakutse.
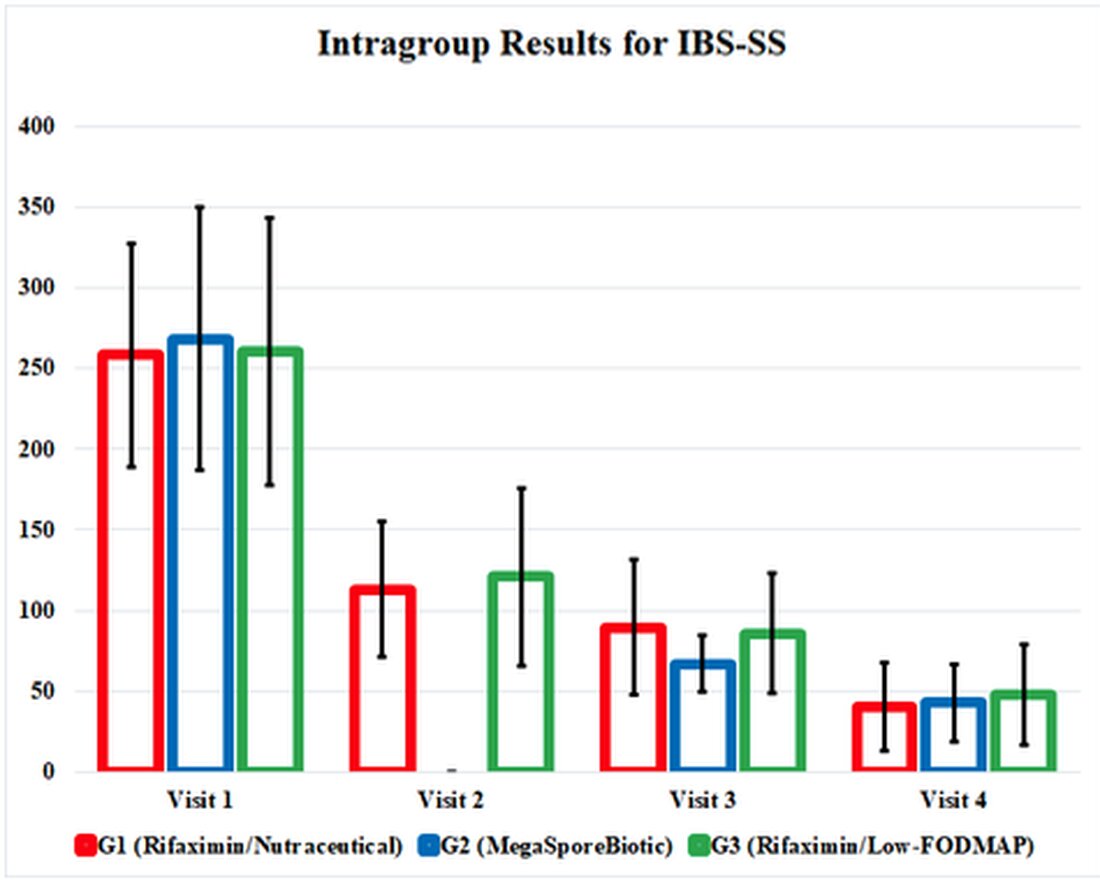
Selle uuringu terapeutiliste sekkumiste mõju maeti segadusse ja kohmakasse tabelitesse, nii et olen uuringu tulemusi illustreeriva graafilise positiivse tulemuse esile toonud. See graafik tutvustab uuringutulemusi ja näitab meile, kui tõhusaid neid ravimeetodeid üksteisega võrreldakse. See rõhutab ka asjaolu, et kõik 3 ravirühma paranesid ka pärast sekkumiste katkestamist visiidil 3 (päev 34).
Selle uuringu üks põnevamaid aspekte on spooripõhiste probiootikumide kulutõhusus võrreldes rifaksimiiniga. Selles uuringus kasutatud rifaksimiini annus maksab umbes 1300 dollarit ja soovitatud annus on lähemal 2000 dollarile. Kindlustuskaitse nõuab sageli ravimite ebaõnnestumisi ja eelnevaid volitusi, kui ravi on üldse kaetud. Selles uuringus kasutatud spooripõhise probiootikumi annus ja kestus on 55 dollarit. See kujutab endast spooripõhist probiootilist ravi olulist eelist. Autorid ei teatanud ühtegi kõrvaltoime ega osalejate väljalangemist, seetõttu on neid tegureid raske arvestada kulutõhususe suhtega.
Samuti tuleb märkida, et tulemused olid spooripõhise probiootilise ravi puhul sarnased võrreldes madala FODMAP-i dieediravi rühmaga. On osutunud tõhusaks toitumisstrateegiaks IBS-D raviks.7Ehkki põnev on IBS-i jaoks tõhus toitumisvahend, on see dieet väga piirav ja sellel on kaugeleulatuv psühhosotsiaalne ja toitumismõju.8Minu kogemuse kohaselt on madal FODMAP -dieet teiste, võib -olla veelgi piiravama dieediga võrreldes stressirohkem dieet, kuna toiduvalikud pole intuitiivsed. Patsiendid peavad pidevalt kasutama jaotusmaterjale ja rakendusi ning seetõttu peavad selle dieedi edukaks järgimiseks olema väga valvsad. Sellega seoses pakub spooripõhine probiootiline teraapia olulist eelist.
Järeldus
Ehkki sellel uuringul on mitmeid metoodilisi probleeme, mis tekitavad eelarvamusi, on oluline mõista, et selle uuringu tulemused parandavad meie arusaamist IBS-D ravivõimalustest. Spoorepõhine probiootiline ravi kui eraldiseisva raviga seostati IBS-i tõsiduse, elukvaliteedi ja rektaalse mahu sensatsiooni paranemist rifaksimiinravi omaga, millele järgnes madala FODMAP-i dieet või probiootiline ravi. Sümptomid paranesid jätkuvalt kõigi 3 sekkumise korral pärast ravi katkestamist, mida tõestavad IBS -i paranenud raskusaste 60. päeval võrreldes 34. päeval pärast ravi katkestamist. Uuringus oli kõige olulisem viga raviks ebapiisav rifaksimiini annus. Sellegipoolest pakub spooripõhine probiootiline teraapia palju lihtsamat ravi vähem kui 5% rifaksimiini maksumusest. Vaja on rohkem uuringuid, enne kui spooripõhine probiootilist ravi võib väita, et see on sama tõhus kui rifaksimiin, kuid kindlasti võib seda kaaluda IBS-D patsientide ravivõimaluste valimisel.

 Suche
Suche
 Mein Konto
Mein Konto