Este artículo es parte de nuestra edición especial de mayo de 2020. Descargue el número completo aquí.
Relación
Catinean A, Neag AM, Nita A, Buzea M, Buzoianu AD.baciloespecies Esporas: una opción de tratamiento prometedora para pacientes con síndrome del intestino irritable.Nutrientes. 2019;11(9):1968.
Objetivo
El objetivo de este estudio fue comparar la rifaximina seguida de una dieta nutracéutica o de oligosacáridos, disacáridos, monosacáridos y polioles de baja fermentación (FODMAP) con la terapia probiótica basada en esporas (MegaSporeBiotic) sola en pacientes con síndrome del intestino irritable (SII) sin estreñimiento.
Borrador
Un ensayo clínico controlado, aleatorizado, prospectivo y no ciego. Los participantes fueron asignados aleatoriamente a 3 grupos:
- G1, bei dem die Teilnehmer eine 10-tägige Kur mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Kur mit einem nutrazeutischen Inhaltsstoff Bifidobacterium longum W11, lösliche Ballaststoffe und Vitamine B1B2B6und B12.
- G2, bei dem die Teilnehmer einen 34-tägigen Kurs erhielten Bazillus spp probiotisch (Bacillus licheniformis, Bacillus indicus HU36™, Bacillus subtilis HU58™, Bacillus clausii, Bacillus coagulansalle von der Marke MegaSporeBiotic).
- G3, bei dem die Teilnehmer eine 10-tägige Behandlung mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Low-FODMAP-Diät.
Los investigadores obtuvieron medidas de resultado al inicio del estudio, el día 10 (para los grupos G1 y G3), el día 34 y el día 60.
Partícipe
Este estudio incluyó a 90 pacientes con síndrome del intestino irritable sin estreñimiento según los criterios de Roma III. Los pacientes tenían entre 18 y 75 años y presentaban colonoscopia normal en los últimos 5 años, valores sanguíneos dentro de valores de referencia y calprotectina fecal normal. Se excluyeron pacientes con alergias alimentarias documentadas, intolerancia al gluten o enfermedad celíaca, diabetes, enfermedad de tiroides, enfermedad inflamatoria intestinal u otras enfermedades orgánicas, trastornos alimentarios (anorexia o bulimia), probióticos 1 mes antes del estudio, tratamiento antibiótico en los últimos 6 meses o dietas específicas.
Parámetros del estudio evaluados.
Los investigadores evaluaron a los pacientes según la puntuación de gravedad del SII (IBS-SS), la calidad de vida de los pacientes con SII (IBS-QL) y una prueba de sensación de volumen rectal.
Ideas clave
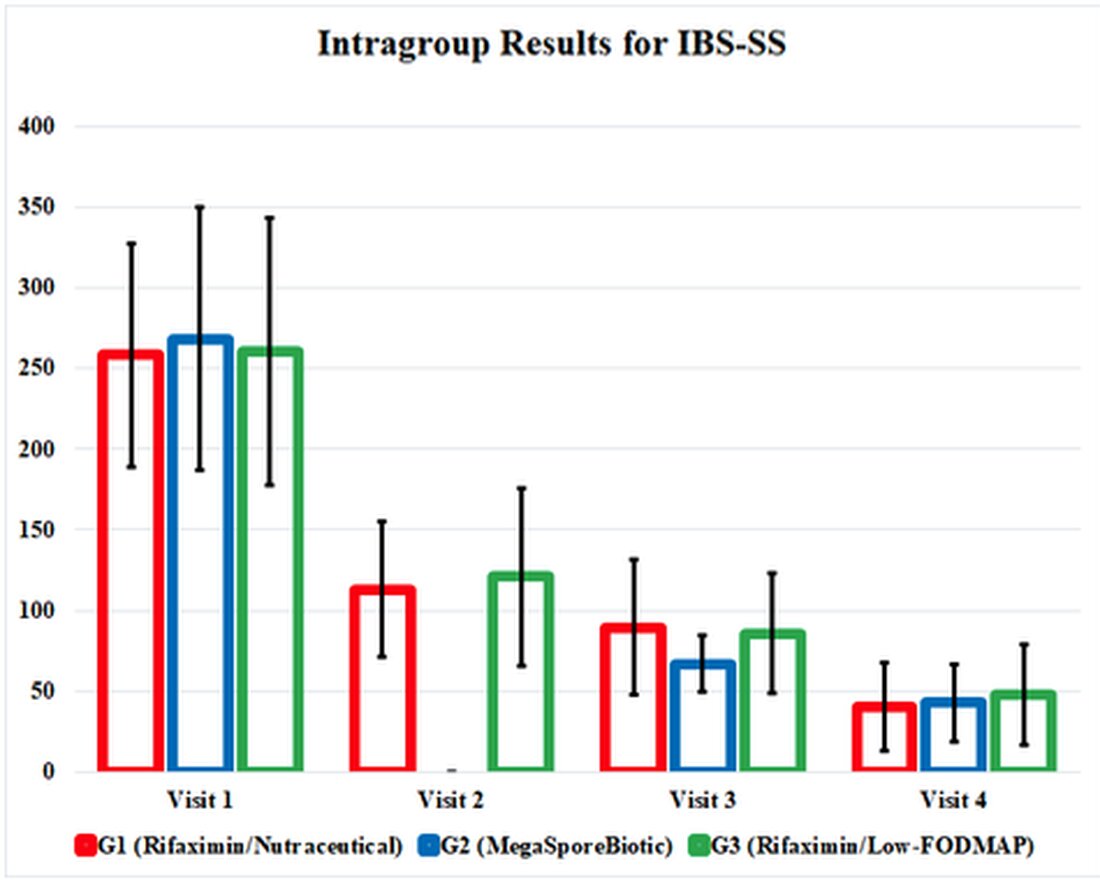
IBS-SS mejoró en todas las medidas de resultado para G1, G2 y G3 y, curiosamente, mejoró igualmente al final del estudio. El grupo MegaSporeBiotic, G2, tuvo una mejoría más temprana de los síntomas en la Visita 3 (día 34). Las puntuaciones de calidad de vida y la prueba de sensación de volumen rectal también mejoraron en cada grupo, con resultados similares en cada grupo.
Implicaciones prácticas
El síndrome del intestino irritable es un trastorno común que afecta aproximadamente al 10% de la población, con importantes lagunas en las estrategias de tratamiento fiables y rentables.1Nuestra comprensión de la fisiopatología se está expandiendo rápidamente utilizando la biología sistémica. El modelo propuesto actualmente es una red compleja de disfunción de la microbiota intestinal, permeabilidad intestinal alterada, motilidad alterada, activación de células inmunes gastrointestinales (GI), hipersensibilidad visceral e interacciones anormales entre el intestino y el cerebro.2La rifaximina surgió por primera vez como una opción de tratamiento eficaz para alterar la microbiota gastrointestinal en 2011 con el ensayo TARGET, que finalmente condujo a la aprobación de la FDA de la rifaximina para el tratamiento del SII con diarrea en 2015.3Este estudio tiene como objetivo demostrar que la terapia sin antibióticos mediante la alteración del microbioma con un probiótico a base de esporas también puede ser eficaz para el tratamiento del SII con diarrea (SII-D).
Uno de los aspectos más interesantes de este estudio es la rentabilidad de los probióticos a base de esporas en comparación con la rifaximina.
Este estudio contiene varias limitaciones importantes, muchas de las cuales los autores reconocen. Estos incluyen la falta de cegamiento y placebo, síntomas moderados en lugar de graves al inicio del estudio, falta de pruebas de aliento para detectar el sobrecrecimiento bacteriano del intestino delgado (SIBO) y el uso de los criterios de Roma III en lugar de los de Roma IV. Los investigadores utilizaron Roma III porque este estudio comenzó antes de Roma IV, y los autores señalan que el 90% de los participantes también cumplieron con los nuevos criterios.
Existen limitaciones adicionales que los autores no discuten. La primera, y quizás la más importante, es que el grupo de tratamiento con rifaximina recibió un tratamiento insuficiente tanto en dosis como en duración. La dosis actualmente generalmente aceptada de rifaximina para el SII-D es de 550 mg 3 veces al día (dosis diaria total de 1650 mg) durante 14 días.4En este estudio se utilizó un total de 1200 mg por día durante 10 días, lo que representa el 52% de la dosis efectiva. Esto conduce a un sesgo de resultados significativo en comparación con la intervención probiótica basada en esporas.
Mejores medidas de resultados podrían fortalecer este estudio. Primero, los autores utilizaron una prueba de sensación de volumen rectal al inicio y en cada visita. Esta prueba es invasiva, inconveniente y tiene poco respaldo en la literatura como medida de resultado para el SII-D.5En lugar de la prueba de sensación de volumen rectal, una prueba de aliento con lactulosa no invasiva de 3 horas mejoraría el diseño del estudio. Esto habría permitido a los autores incluir solo pacientes con SIBO o estratificar a los respondedores en cada grupo de tratamiento según el estado de SIBO. Rezaie et al. encontraron que los pacientes con una prueba de aliento con lactulosa positiva para SIBO respondieron significativamente mejor a la terapia con rifaximina que los pacientes con SII-D con una prueba de aliento normal.6La inclusión de una prueba de aliento con lactulosa de 3 horas en este estudio habría aclarado qué pacientes eran los mejores candidatos para el tratamiento con probióticos a base de esporas versus la terapia con rifaximina.
El uso de 2 grupos de tratamiento (rifaximina/dieta baja en FODMAP versus probiótico a base de esporas) o 2 grupos de tratamiento y un grupo de placebo habría mejorado la claridad de los resultados. El cegamiento podría eliminar otra fuente de sesgo; Sin embargo, es imposible cegar la nutrición terapéutica a la nutrición habitual y este es un desafío continuo en la investigación nutricional.
Los efectos de las intervenciones terapéuticas en este estudio quedaron enterrados en tablas confusas y engorrosas, por lo que he resaltado los resultados positivos en un gráfico que ilustra los resultados del estudio. Este gráfico presenta los resultados del estudio y nos muestra cuán efectivas son estas terapias comparadas entre sí. También destaca el hecho de que los 3 grupos de tratamiento continuaron mejorando incluso después de que se suspendieron las intervenciones en la Visita 3 (Día 34).
Uno de los aspectos más interesantes de este estudio es la rentabilidad de los probióticos a base de esporas en comparación con la rifaximina. La dosis de rifaximina utilizada en este estudio cuesta aproximadamente $1300 y la dosis recomendada se acerca a los $2000. La cobertura del seguro a menudo requiere múltiples fallas de medicación y autorizaciones previas si es que el tratamiento está cubierto. La dosis y la duración del probiótico a base de esporas utilizado en este estudio se vende por $55. Esto representa una ventaja significativa de la terapia con probióticos basada en esporas. Los autores no informaron ningún efecto secundario ni abandonos de los participantes, por lo que es difícil tener en cuenta estos factores en una relación costo-efectividad.
También cabe señalar que los resultados fueron similares para la terapia con probióticos a base de esporas en comparación con el grupo de tratamiento con dieta baja en FODMAP. Se ha demostrado que la dieta baja en FODMAP es una estrategia nutricional eficaz para tratar el SII-D.7Aunque es emocionante tener una herramienta nutricional eficaz para el SII, esta dieta es muy restrictiva y tiene efectos psicosociales y nutricionales de gran alcance.8En mi experiencia, la dieta baja en FODMAP es una dieta más estresante en comparación con otras dietas, quizás incluso más restrictivas porque la elección de alimentos no es intuitiva. Los pacientes deben utilizar constantemente folletos y aplicaciones y, por lo tanto, deben estar muy atentos para seguir esta dieta con éxito. En este sentido, la terapia con probióticos basada en esporas ofrece una ventaja significativa.
Conclusión
Aunque este estudio tiene varios problemas metodológicos que introducen sesgos, es importante reconocer que los resultados de este estudio mejoran nuestra comprensión de las opciones de tratamiento para el SII-D. La terapia con probióticos a base de esporas como terapia independiente se asoció con mejoras en la gravedad del SII, la calidad de vida y la sensación de volumen rectal equivalentes a las de la terapia con rifaximina seguida de una dieta baja en FODMAP o una terapia con probióticos. Los síntomas continuaron mejorando en las 3 intervenciones después de la interrupción del tratamiento, como lo demuestran las mejores puntuaciones de gravedad del SII en el día 60 en comparación con el día 34 después de la interrupción del tratamiento. El error más significativo del estudio fue la dosis insuficiente de rifaximina para el tratamiento. Sin embargo, la terapia con probióticos a base de esporas ofrece un tratamiento mucho más sencillo por menos del 5% del coste de la rifaximina. Se necesita más investigación antes de que se pueda afirmar que la terapia con probióticos basada en esporas es tan efectiva como la rifaximina, pero ciertamente se puede considerar al seleccionar opciones de tratamiento para pacientes con SII-D.

 Suche
Suche
 Mein Konto
Mein Konto