Denne artikel er en del af vores specielle maj 2020 -udgave. Download det fulde problem her.
Forhold
Catinean A, Neag AM, Nita A, Buzea M, Buzoianu AD.Bacillusspp. Sporer - En lovende behandlingsmulighed for patienter med irritabelt tarmsyndrom.Næringsstoffer. 2019; 11 (9): 1968.
Objektiv
Formålet med denne undersøgelse var at sammenligne rifaximin efterfulgt af en ernæringsmæssig eller lav fermenterbar oligosaccharid, disaccharid, monosaccharid og polyol (FODMAP) diæt med sporbaseret probiotikum (megasporebiotisk) terapi alene hos patienter med irritabel towel syndrom (IBS) uden forstærkning.
Udkast
Et ikke-blindet, potentielt, randomiseret, kontrolleret klinisk forsøg. Deltagerne blev randomiseret i 3 grupper:
- G1, bei dem die Teilnehmer eine 10-tägige Kur mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Kur mit einem nutrazeutischen Inhaltsstoff Bifidobacterium longum W11, lösliche Ballaststoffe und Vitamine B1B2B6und B12.
- G2, bei dem die Teilnehmer einen 34-tägigen Kurs erhielten Bazillus spp probiotisch (Bacillus licheniformis, Bacillus indicus HU36™, Bacillus subtilis HU58™, Bacillus clausii, Bacillus coagulansalle von der Marke MegaSporeBiotic).
- G3, bei dem die Teilnehmer eine 10-tägige Behandlung mit Rifaximin (1.200 mg) erhielten, gefolgt von einer 24-tägigen Low-FODMAP-Diät.
Forskere opnåede resultatmålinger ved baseline, dag 10 (for grupper G1 og G3), dag 34 og dag 60.
Deltager
Denne undersøgelse omfattede 90 patienter med irritabelt tarmsyndrom uden forstoppelse baseret på Rom III -kriterierne. Patienterne var mellem 18 og 75 år gamle og havde en normal koloskopi i de sidste 5 år, blodværdier inden for referenceværdier og normal fækal calprotectin. Patienter med dokumenterede fødevareallergi, glutenintolerance eller cøliaki, diabetes, skjoldbruskkirtelsygdom, inflammatorisk tarmsygdom eller andre organiske sygdomme, spiseforstyrrelser (anoreksi eller bulimi), probiotika 1 måned før undersøgelsen, antibiotisk behandling i de sidste 6 måneder eller specifikke diæter blev udelukket.
Undersøgelsesparametre vurderet
Forskere evaluerede patienter baseret på IBS-sværhedsgrad (IBS-SS), livskvalitet for IBS-patienter (IBS-QL) og en rektal volumen-sensationstest.
Nøgleindsigt
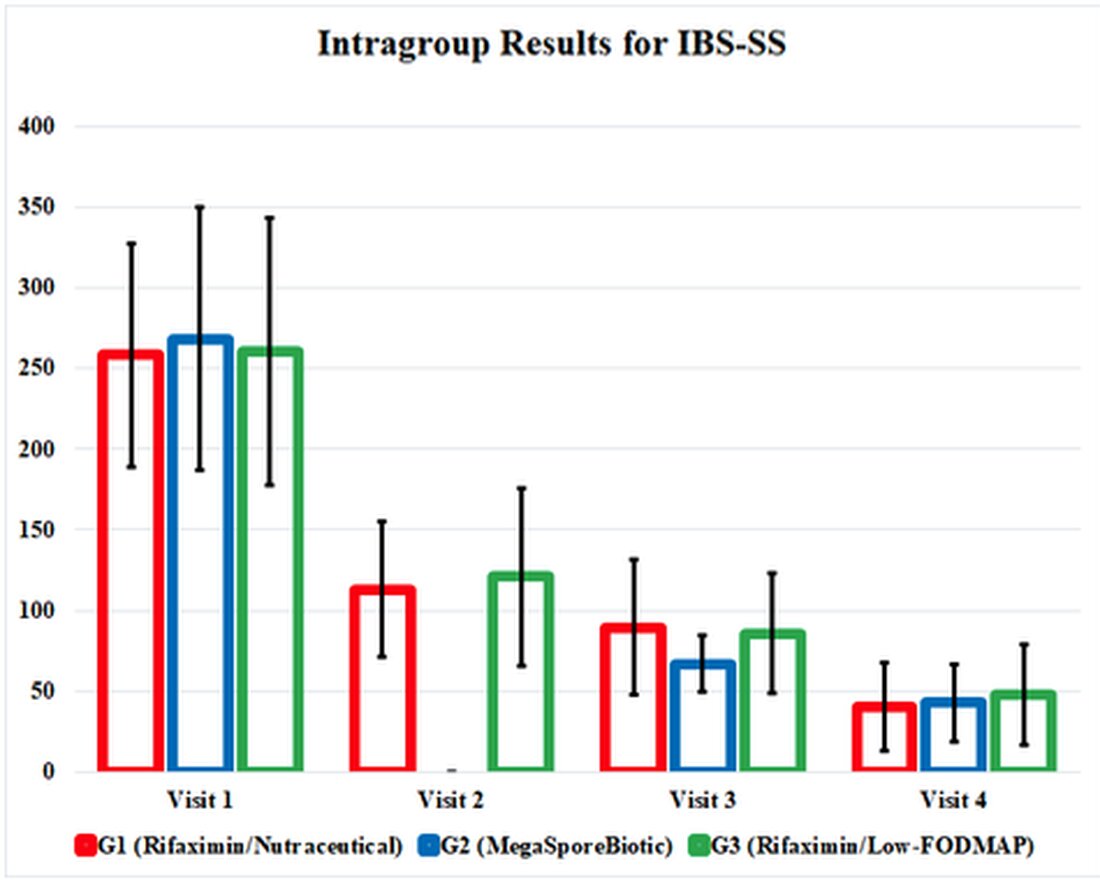
IBS-SS forbedrede sig ved ethvert resultatmål for G1, G2 og G3 og forbedrede interessant nok lige ved afslutningen af undersøgelsen. Den megasporebiotiske gruppe, G2, havde tidligere symptomforbedring ved besøg 3 (dag 34). Livskvalitetsresultater og rektal volumenfølelse test forbedrede sig også i hver gruppe med lignende resultater i hver gruppe.
Øv konsekvenser
Irritabelt tarmsyndrom er en almindelig lidelse, der påvirker ca. 10% af befolkningen, med betydelige huller i pålidelige og omkostningseffektive behandlingsstrategier.1Vores forståelse af patofysiologi ekspanderer hurtigt ved hjælp af systemisk biologi. Den aktuelt foreslåede model er et komplekst web af tarmmikrobiota-dysfunktion, ændret tarmpermeabilitet, ændret motilitet, gastrointestinal (GI) immuncelleaktivering, visceral overfølsomhed og unormale tarm-hjerne-interaktioner.2Rifaximin fremkom først som en effektiv behandlingsmulighed til ændring af GI -mikrobiotaen i 2011 med målforsøget, hvilket i sidste ende førte til FDA -godkendelse af rifaximin til behandling af IBS med diarré i 2015.3Denne undersøgelse sigter mod at vise, at ikke-antibiotisk terapi ved at ændre mikrobiomet med et sporbaseret probiotikum også kan være effektiv til behandling af IBS med diarré (IBS-D).
Et af de mest spændende aspekter af denne undersøgelse er omkostningseffektiviteten af sporbaserede probiotika sammenlignet med rifaximin.
Denne undersøgelse indeholder adskillige signifikante begrænsninger, hvoraf mange anerkender. Disse inkluderer en mangel på blinding og placebo, moderat snarere end alvorlige symptomer ved baseline, en mangel på åndedrætsprøvning for tyndtarmsbakteriel overvækst (SIBO) og brugen af Rom III snarere end Rom IV -kriterier. Forskerne brugte Rom III, fordi denne undersøgelse begyndte før Rom IV, og forfatterne bemærker, at 90% af deltagerne også opfyldte de nye kriterier.
Der er yderligere begrænsninger, der ikke drøftes af forfatterne. Den første og måske vigtigste er, at rifaximinbehandlingsgruppen blev underbehandlet i både dosis og varighed. Den i øjeblikket generelt accepterede dosering af rifaximin for IBS-D er 550 mg 3 gange dagligt (1.650 mg total daglig dosis) i 14 dage.4I denne undersøgelse blev i alt 1.200 mg pr. Dag anvendt i 10 dage, hvilket er 52% af den effektive dosis. Dette fører til en signifikant resultatforspænding sammenlignet med den sporbaserede probiotiske intervention.
Forbedrede resultatmålinger kunne styrke denne undersøgelse. Først brugte forfatterne en rektal volumen sensationstest ved baseline og ved hvert besøg. Denne test er invasiv, ubelejlig og har lidt støtte i litteraturen som et resultatmål for IBS-D.5I stedet for rektalvolumen-sensationstest, ville en ikke-invasiv 3-timers lactulose-åndedrætsprøve forbedre undersøgelsesdesignet. Dette ville have gjort det muligt for forfatterne kun at inkludere patienter med SIBO eller at stratificere respondenter i hver behandlingsgruppe baseret på SIBO -status. Rezaie et al. fandt, at patienter med en positiv lactulose-åndedrætsprøve for SIBO reagerede signifikant bedre på rifaximinbehandling end IBS-D-patienter med en normal åndedrætsprøve.6Inkludering af en 3-timers lactulose-åndedrætsprøve i denne undersøgelse ville have afklaret, hvilke patienter der var de bedste kandidater til sporbaseret probiotisk behandling versus rifaximinbehandling.
Anvendelsen af 2 behandlingsgrupper (Rifaximin/Low-FodMap-diæt versus spore-baseret probiotikum) eller 2 behandlingsgrupper og en placebogruppe ville have forbedret resultaterne af resultaterne. Blinding kunne eliminere en anden kilde til bias; Det er dog umuligt at blinde terapeutisk ernæring til sædvanlig ernæring, og dette er en løbende udfordring inden for ernæringsmæssig forskning.
Virkningerne af de terapeutiske interventioner i denne undersøgelse blev begravet i forvirrende og besværlige tabeller, så jeg har fremhævet positive resultater i en grafik, der illustrerer undersøgelsens resultater. Denne grafiske præsenterer undersøgelsesresultaterne og viser os, hvor effektive disse terapier sammenlignes med hinanden. Det fremhæver også det faktum, at alle 3 behandlingsgrupper fortsatte med at forbedre sig, selv efter at interventioner blev afbrudt ved besøg 3 (dag 34).
Et af de mest spændende aspekter af denne undersøgelse er omkostningseffektiviteten af sporbaserede probiotika sammenlignet med rifaximin. Rifaximin -dosis, der blev anvendt i denne undersøgelse, koster cirka $ 1.300, og den anbefalede dosis er tættere på $ 2.000. Forsikringsdækning kræver ofte flere medicinfejl og forudgående tilladelser, hvis behandling overhovedet dækkes. Dosis og varighed af det sporbaserede probiotikum, der blev anvendt i denne undersøgelse, retails for $ 55. Dette repræsenterer en betydelig fordel ved sporbaseret probiotikabehandling. Forfatterne rapporterede ikke om nogen bivirkninger eller deltageraffald, så det er vanskeligt at faktorere disse faktorer i et omkostningseffektivitetsforhold.
Det skal også bemærkes, at resultaterne var ens for sporbaseret probiotikabehandling sammenlignet med gruppen med lavt fodmap-diæt. Diæt med lavt fodmap har vist sig at være en effektiv ernæringsstrategi til behandling af IBS-D.7Selvom det er spændende at have et effektivt ernæringsværktøj til IBS, er denne diæt meget restriktiv og har vidtrækkende psykosociale og ernæringsmæssige effekter.8Efter min erfaring er den lave FODMAP -diæt en mere stressende diæt sammenlignet med andre, måske endnu mere restriktive diæter, fordi fødevarevalg ikke er intuitive. Patienter skal konstant bruge uddelinger og apps og skal derfor blive meget årvågen for at følge denne diæt med succes. I denne henseende tilbyder sporebaseret probiotisk terapi en betydelig fordel.
Konklusion
Selvom denne undersøgelse har flere metodologiske problemer, der introducerer bias, er det vigtigt at erkende, at resultaterne af denne undersøgelse forbedrer vores forståelse af behandlingsmuligheder for IBS-D. Spore-baseret probiotisk terapi som en selvstændig terapi var forbundet med forbedringer i IBS-sværhedsgrad, livskvalitet og rektal volumenfølelse svarende til dem med rifaximinbehandling efterfulgt af en lav-fodmap diæt eller probiotisk terapi. Symptomerne blev fortsat forbedret for alle 3 interventioner efter seponering af behandlingen, hvilket fremgår af forbedrede IBS -sværhedsgrad på dag 60 sammenlignet med dag 34 efter seponering af behandlingen. Den mest markante fejl i undersøgelsen var den utilstrækkelige dosis af rifaximin til behandling. Ikke desto mindre tilbyder sporebaseret probiotisk terapi en meget enklere behandling til mindre end 5% af omkostningerne ved rifaximin. Mere forskning er nødvendig, før spore-baseret probiotikabehandling kan hævdes at være lige så effektiv som rifaximin, men det kan bestemt overvejes, når man vælger behandlingsmuligheder for IBS-D-patienter.

 Suche
Suche
 Mein Konto
Mein Konto