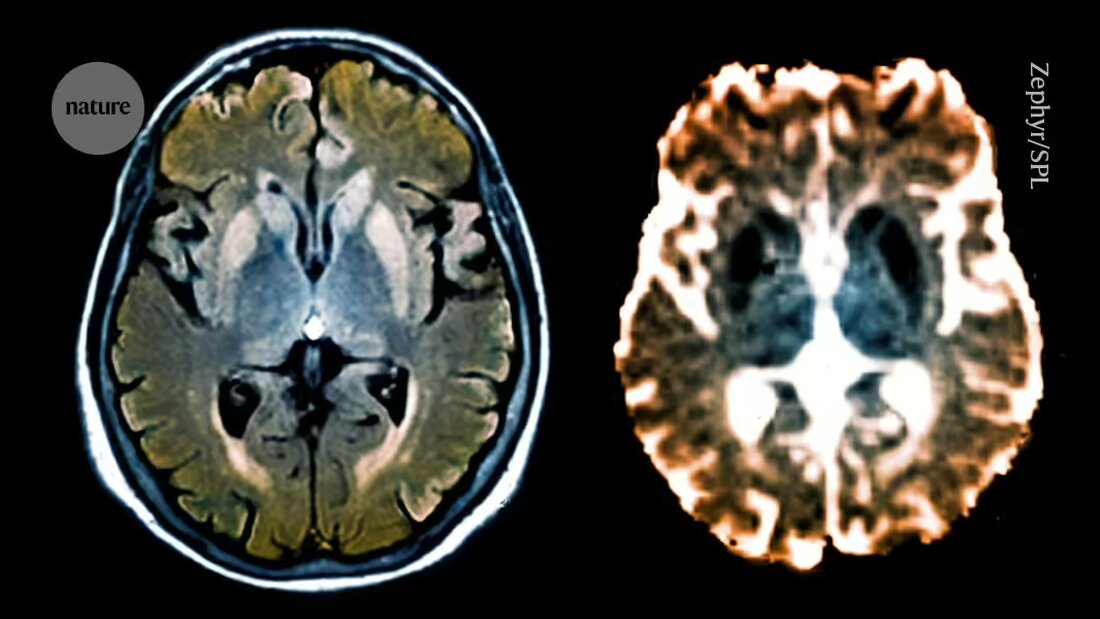
Alat za molekularno uređivanje dovoljno malen da se može isporučiti u mozak zaustavlja proizvodnju proteina koji uzrokuju prionske bolesti, rijetku, ali smrtonosnu skupinu neurodegenerativnih poremećaja.
Sustav – poznat kao “spareni histonski rep za automatsko otpuštanje metiltransferaze (CHARM)” – mijenja 'epigenom', skup kemijskih oznaka povezanih s DNK koje utječu na aktivnost gena. U miševa je CHARM utišao gen koji proizvodi štetne proteine koji uzrokuju prionske bolesti u većini neurona u mozgu, bez promjene sekvence gena.
CHARM je prvi korak prema razvoju sigurnog i učinkovitog "jednokratnog tretmana" za smanjenje razine proteina koji uzrokuju bolest, kaže Madelynn Whittaker, bioinženjer na Sveučilištu Pennsylvania u Philadelphiji. Rezultati su objavljeni danasZnanost 1objavljeno.
"Sustav se bavi značajnim izazovima s kojima su se suočavali prethodni sustavi epigenetskog uređivanja", kaže Whittaker, prateći perspektivni članak uZnanostu koautorstvu. To uključuje smanjenje toksičnosti alata za uređivanje i njihovu isporuku stanicama bez ugrožavanja njihove učinkovitosti, dodaje ona.
Prionske bolesti uzrokuju pogrešno savijeni prionski proteini (PrP) koji se skupljaju i uništavaju neurone. To može dovesti do stanja poput fatalnog sindroma obiteljske nesanice - rijetke genetske bolesti koja sprječava ljude da spavaju i dovodi do smrti. Iako su prionske bolesti neizlječive, lijekovi koji se nazivaju antisense oligonukleotidi (ASO) pokazali su neke obećavajuće rezultate. Ove kratke, jednolančane molekule vežu se na neispravne sekvence glasničke RNA i povećavaju ili smanjuju ekspresiju proteina. Prethodne studije na miševima zaraženim pogrešno presavijenim verzijama PrP-a pokazale su da ASO smanjuju ekspresiju ovih proteina i produžuju životni vijek 2. Ali lijekovi zahtijevaju višestruke injekcije kako bi se postigao dugoročni terapeutski učinak i mogu dovesti do nuspojava kao što je oštećenje jetre, kaže Whittaker.
Godine 2021. Jonathan Weissman, biokemičar s Massachusetts Institute of Technology u Cambridgeu, i njegov tim razvili su CRISPRoff 3– alat za uređivanje koji dodaje kemijsku oznaku zvanu metilna skupina na lanac DNK, što smanjuje aktivnost gena bez mijenjanja genoma. Ali alat se ne može isporučiti do moždanih stanica jer su njegove genetske komponente prevelike da stanu u adeno-povezani virus (AAV) - uobičajeno sredstvo za isporuku genske terapije u stanice. “Pravi izazov bila je isporuka”, kaže Weissman.
Novi urednik
Kako bi to riješili, Weissman i njegov tim razvili su CHARM, koji koristi molekule zvane proteini cinkovog prsta kako bi se usmjerio na ciljane gene. Ti su proteini dovoljno mali da se isporuče u AAV vektoru.
Istraživači su modificirali CHARM kako bi regrutirao i aktivirao komponente DNA metiltransferaza - molekula koje se nalaze u stanicama koje pričvršćuju metilne skupine na DNA, uzrokujući promjenu ekspresije gena. Time se smanjuju toksični učinci povezani s dodavanjem molekula izvan stanice, kaže Weissman. "Jedina stvar koju smo promijenili u stanici bila je njezina sposobnost ekspresije prionskog proteina", kaže on.
Kada su istraživači isporučili CHARM u mozgove zdravih miševa, otkrili su da je smanjio ekspresiju PrP-a u mozgu za više od 80% - znatno iznad minimalne razine potrebne za terapeutski učinak. Weissman i njegov tim također su dizajnirali CHARM da se isključi nakon što završi svoj tihi rad, sprječavajući ga da sam sebe kopira što bi moglo dovesti do štetnih nuspojava.
Tim koji stoji iza CHARM-a uključuje Sonia Vallabh i njezinog supruga Erica Vallabha Minikela, znanstvenike za prione na Broad institutu MIT-a i Sveučilišta Harvard u Cambridgeu. Vallabh je naslijedio mutaciju iza sindroma fatalne obiteljske nesanice, a prije dvanaest godina Vallabh i Minikel zamijenili su karijeru kako bi istražili načine liječenja ove bolesti. Vallabh kaže da joj CHARM donosi "ogromno samopouzdanje". Ona dodaje da je razvoj lijekova obično spor, ali rad pokazuje koliko se brzo mogu razviti novi pristupi uz pravi tim. “Razmjer onoga što možete postići u kratkom vremenskom razdoblju je nevjerojatan,” kaže Vallabh. "Prije samo dvije godine i mjesec dana prvi put smo predstavili Jonathanu ideju o zajedničkoj suradnji i sada smo tu."
CHARM također ima potencijal za liječenje drugih bolesti uzrokovanih nakupljanjem abnormalnih proteina, kao što su Parkinsonova i Alzheimerova bolest, dodaje Weissman. "Znamo da epigenetsko utišavanje ne funkcionira za svaki gen, već za većinu gena", kaže on.
Jacob Goell, istraživač koji razvija alate za uređivanje epigenoma na Sveučilištu Rice u Houstonu, Texas, optimističan je da će CHARM jednog dana završiti u klinici. Ali potreban je sveobuhvatniji rad kako bi se procijenilo kako alat i promjene koje stvara komuniciraju s genetskim strojevima stanica, osobito tijekom dužih vremenskih razdoblja, dodaje.
Sljedeći korak je proučavanje kako CHARM radi u AAV vektoru koji može ciljati neurone u ljudskom mozgu. "Ovo je sljedeći veliki izazov", kaže.

 Suche
Suche
 Mein Konto
Mein Konto