Rasprava o lijeku za Alzheimerovu bolest lecanemab - jednom od prvih lijekova za usporavanje kognitivnog pada kod ljudi - intenzivira se među istraživačima i kliničarima o tome nadmašuju li potencijalne koristi liječenja rizike.
Dana 22. kolovoza britanska Regulatorna agencija za lijekove i zdravstvene proizvode dala je zeleno svjetlo lijeku. U isto vrijeme, međutim, britanski zdravstveni regulator NICE, koji određuje hoće li se lijekovi nuditi pacijentima u britanskom Državnom zdravstvenom servisu (NHS), rekao je u nacrtu da lekanemab neće biti dostupan na NHS-u jer su dobrobiti premale da bi opravdale visoke troškove.
"Neobično dugo vremena koje su proveli pregledavajući lijek sugerira da to nije bila laka ni jednostavna odluka", rekao je psihijatar Robert Howard sa Sveučilišta u Londonu u izjavi za Science Media Center u Britaniji.
Američki regulatori prvi su odobrili lijek 2023. godine, a Europska agencija za lijekove (EMA) sada preispituje svoju odluku nakon žalbe proizvođača lijekova.
Amiloidna meta
Odluka EMA-e također je izazvala različite reakcije zajednice oboljelih od Alzheimera. "Ovdje su emocije stvarno uzburkane", kaže biokemičar Christian Haass sa Sveučilišta Ludwig Maximilians u Münchenu, Njemačka, koji se ne slaže s ovom odlukom. "To je prvi lijek koji mijenja bolest koji imamo u više od 30 godina." Uskraćivanje pacijentima pristupa lekanemabu znači da mnogi gube priliku da dobiju dragocjeno vrijeme, prema Haassu.
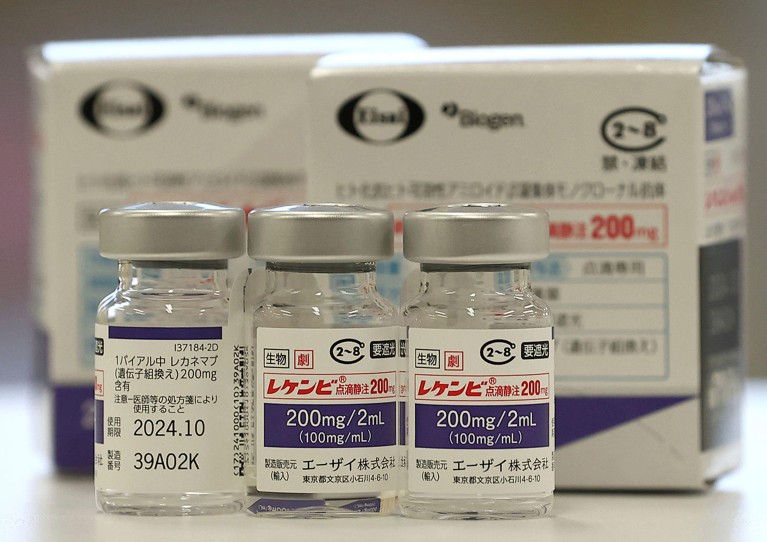
Lecanemab ili Leqembi je monoklonsko protutijelo koje eliminira amiloid, tvar koja se nakuplja u otrovne nakupine u mozgu ljudi s Alzheimerovom bolešću. Lijek, koji proizvode Eisai u Tokiju i Biogen u Cambridgeu, Massachusetts, također je odobren u Kini, Japanu, Južnoj Koreji i Ujedinjenim Arapskim Emiratima.
Drugi plješću EMA-i, rekavši da iako je lijek bio učinkovit u smanjenju razine amiloida u mozgu, ostaje nejasno hoće li rezultirajuće smanjenje kognitivnog pada rezultirati klinički relevantnim dobrobitima za pacijente. Oni navode da je mogućnost ozbiljnih komplikacija kao što su krvarenje ili oteklina u mozgu uzrokovana nuspojavom koja se zove amiloidni slikovni efekti (ARIA), iako mala, velika zabrinutost. “Razumna procjena rizika u odnosu na dobrobiti ovog lijeka trebala bi navesti ljude da budu vrlo skeptični”, kaže Matthew Schrag, neurolog sa Sveučilišta Vanderbilt u Nashvilleu, Tennessee.
Skromni učinci
Dugo se raspravlja o tome da li lekanemab primijenjen putem infuzije ljudima osigurava klinički značajna smanjenja kognitivnog pada.
Faza III kliničkog ispitivanja lijeka, objavljena 2022. godine, uključila je 1795 ljudi u ranoj fazi Alzheimerove bolesti i otkrila da su oni koji su primili lijek pokazali smanjenje kognitivnog pada za 27% nakon 18 mjeseci u usporedbi s onima koji su primili placebo. Neki su istraživači tu vijest proslavili kao pobjedu na terenu. Međutim, drugi su tvrdili da su učinci premali da bi imali značajan utjecaj na pacijente.
Jedan od razloga za ovu razliku u perspektivi je način na koji ljudi gledaju na podatke, kaže Sebastian Walsh, istraživač javnog zdravlja na Sveučilištu Cambridge, UK. Smanjenje od 27% predstavlja relativnu razliku u količini kognitivnog pada koju je doživjela skupina koja je primala lijek u usporedbi s placebo grupom. Međutim, apsolutna razlika u kognitivnoj funkciji puno je manja: 0,45 bodova na ljestvici od 18 stupnjeva. "Ljudi mogu izdvojiti što god žele iz veličine efekta", kaže Walsh. "Ako žele prodati lijek, mogli bi se usredotočiti na relativne promjene - a ako su jako skeptični, mogli bi govoriti o apsolutnim razlikama."
Ali čak i mali učinci mogu postati značajni tijekom vremena, osobito u kasnijim fazama bolesti kada se razgradnja događa brže, kaže Walsh. "U konačnici ovisi o tome što mislite kakav će biti dugoročni učinak, a mi na to nemamo odgovor."
Sada su dostupni neki dugoročni podaci. Na Međunarodnoj konferenciji Alzheimer Association (AAIC) u Philadelphiji prošlog mjeseca, Eisai i Biogen predstavili su rezultate otvorene proširene studije koja je nastavila pratiti pacijente koji su primali lekanemab nakon završetka ispitivanja faze III. Nakon tri godine kontinuiranog liječenja više od polovice pacijenata pokazalo je poboljšanje, a većina slučajeva ARIA-e javila se u prvih šest mjeseci liječenja. Također su izvijestili da se stopa kognitivnog pada vratila na razinu placeba kada su ljudi prestali uzimati lijek, čak i ako su amiloidni plakovi uklonjeni prije prekida liječenja.
Neki su optimistični u pogledu ovih rezultata - Haass kaže da je uzbudljivo vidjeti da lijek ne samo da eliminira amiloid, već i usporava širenje taua, još jednog proteina koji se nakuplja u nakupine u mozgovima ljudi s Alzheimerom. Drugi su oprezniji. Paresh Malhotra, neurolog s Imperial Collegea u Londonu, ističe da pozitivni rezultati predstavljeni na AAIC-u nisu uspoređivani s placebom pa je potrebno više podataka kako bi se utvrdila dugoročna učinkovitost lijeka.
Trošak je također problem. Walsh kaže da je, s obzirom na skromne učinke lijeka, teško opravdati troškove primjene lijeka (koji u SAD-u košta više od 20.000 dolara godišnje) i potrebne postupke, poput snimanja i genetskog testiranja, da se identificiraju osobe koje ispunjavaju uvjete da ga prime.
Zabrinutost za sigurnost
Najveća zabrinutost kod lekanemaba je ARIA, na što je američka Agencija za hranu i lijekove (FDA) upozorila u svom odobrenju. Iako je većina slučajeva asimptomatska - a niti jedan nije prijavljen tijekom početnog 18-mjesečnog kliničkog ispitivanja - bilo je nekih smrtnih slučajeva povezanih s ARIA-om u produženoj fazi studije.
Neki stručnjaci kažu da iako je rizik od ozbiljne ARIA nizak, također je važno uzeti u obzir da se lijek daje u najranijim fazama Alzheimerove bolesti. “Ovo je razdoblje u kojem ljudi imaju najviše za izgubiti”, kaže Schrag. "Tijekom ovog prozora često potičemo pacijente da putuju, razmisle o svom popisu i ostvare stvari koje žele postići u životu."
Ellis van Etten, neurolog s Leidenskog sveučilišnog medicinskog centra u Nizozemskoj, kaže da još uvijek ima mnogo neodgovorenih pitanja o ARIA-i i kako bi liječnici trebali reagirati kada vide da pacijenti razvijaju te abnormalnosti tijekom liječenja. Na primjer: Tko će razviti ozbiljnu ili po život opasnu ARIA? U kojem trenutku ARIA prelazi iz bezopasne u štetnu i kada treba prekinuti liječenje lekanemabom?
Mnoga od istih pitanja o prednostima i rizicima također se odnose na drugo protutijelo za čišćenje amiloida, donanemab - koji proizvodi Eli Lilly u Indianapolisu, Indiana - koje je odobrila FDA u srpnju. Čini se da donanemab pruža približno isto smanjenje kognitivnog pada kao i lekanamab – i povezan je sa smrtnim slučajevima povezanim s ARIA-om.
"Iz rada na biomarkerima znamo da ta antitijela čiste amiloid, tako da znamo da se bave temeljnim mehanizmom bolesti", kaže Malhotra. No ti lijekovi sami po sebi vjerojatno neće biti dovoljni, a bit će važno pozabaviti se i drugim aspektima bolesti. "Vrlo je vjerojatno da ćemo za 10 godina govoriti o kombiniranim terapijama i da će uklanjanje amiloida biti dio tog pristupa."

 Suche
Suche
 Mein Konto
Mein Konto