Arutelu Alzheimeri tõve ravimi lekanemabi üle, mis on üks esimesi ravimeid, mis aeglustab inimeste kognitiivset langust, on teadlaste ja arstide seas intensiivistumas selle üle, kas ravi potentsiaalne kasu kaalub üles sellega kaasnevad riskid.
22. augustil andis Suurbritannia ravimite ja tervishoiutoodete reguleeriv amet ravimile rohelise tule. Samal ajal aga teatas Suurbritannia tervishoiuregulaator NICE, mis määrab, kas Briti riigi rahastatava riikliku tervishoiuteenistuse (NHS) kaudu patsientidele ravimeid pakutakse, eelnõus, et lekanemabi ei tehta NHS-ile kättesaadavaks, kuna sellest saadav kasu on liiga väike, et õigustada kõrgeid kulusid.
"Ebatavaliselt pikk aeg, mille nad kulutasid ravimi ülevaatamisele, viitab sellele, et see ei olnud kerge ega lihtne otsus," ütles Londoni ülikooli kolledži psühhiaater Robert Howard Suurbritannias Science Media Centerile antud avalduses.
USA reguleerivad asutused kiitsid ravimi esimesena heaks 2023. aastal ning Euroopa Ravimiamet (EMA) vaatab nüüd oma otsust pärast ravimitootja apellatsiooni läbi.
Amüloidi sihtmärk
EMA otsus pälvis ka Alzheimeri kogukonnas vastakaid reaktsioone. "Emotsioonid on siin tõesti laes," ütleb Saksamaal Müncheni Ludwig Maximiliansi ülikooli biokeemik Christian Haass, kes ei nõustu otsusega. "See on esimene haigust modifitseeriv ravim rohkem kui 30 aasta jooksul." Haassi sõnul tähendab patsientide juurdepääsu keelamine lekanemabile, et paljud kaotavad võimaluse väärtuslikku aega võita.
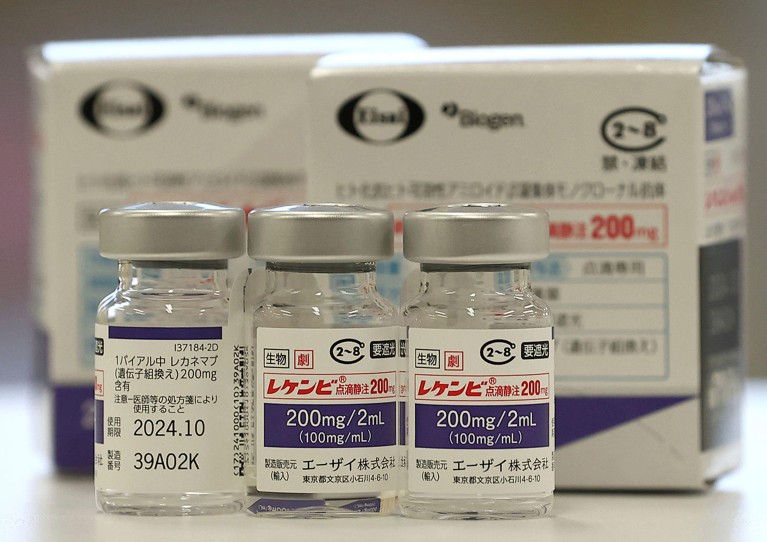
Lecanemab ehk Leqembi on monoklonaalne antikeha, mis kõrvaldab amüloidi – aine, mis ladestub Alzheimeri tõvega inimeste ajus toksilisteks tükkideks. Tokyos Eisai ja Massachusettsi osariigis Cambridge'is Biogeni valmistatud ravim on heaks kiidetud ka Hiinas, Jaapanis, Lõuna-Koreas ja Araabia Ühendemiraatides.
Teised kiidavad EMA-le, öeldes, et kuigi ravim on olnud tõhus aju amüloiditaseme vähendamisel, jääb ebaselgeks, kas sellest tulenev kognitiivse languse vähenemine toob patsientidele kliiniliselt olulist kasu. Nad väidavad, et tõsiste tüsistuste, nagu verejooks või ajuturse, põhjustatud kõrvaltoimest, mida nimetatakse amüloidiga seotud kujutise mõjudeks (ARIA), on suur probleem, kuigi see on väike. "Selle ravimi riskide ja eeliste mõistlik hindamine peaks panema inimesed olema väga skeptilised," ütleb Tennessee osariigis Nashville'is asuva Vanderbilti ülikooli neuroloog Matthew Schrag.
Tagasihoidlikud efektid
Pikka aega on vaieldud selle üle, kas infusioonina manustatud lekanemab vähendab inimestel kliiniliselt olulist kognitiivset langust.
Ravimi III faasi kliiniline uuring, mis avaldati 2022. aastal, hõlmas 1795 Alzheimeri tõve algstaadiumis inimest ja leidis, et nendel, kes said seda ravimit, vähenes kognitiivne langus pärast 18 kuud 27% võrreldes platseebot saanud inimestega. Mõned teadlased tähistasid uudist valdkonna võiduna. Teised aga väitsid, et mõju on liiga väike, et avaldada patsientidele olulist mõju.
Üheks selle erinevuse põhjuseks on see, kuidas inimesed andmeid vaatavad, ütleb Ühendkuningriigi Cambridge'i ülikooli rahvatervise uurija Sebastian Walsh. 27% vähenemine näitab suhtelist erinevust ravimirühmas kogetud kognitiivse languse ulatuses võrreldes platseeborühmaga. Kognitiivse funktsiooni absoluutne erinevus on aga palju väiksem: 0,45 punkti 18-pallisel skaalal. "Inimesed saavad efekti suurusest välja võtta mida iganes nad tahavad," ütleb Walsh. "Kui nad tahavad ravimit müüa, võiksid nad keskenduda suhtelistele muutustele ja kui nad on väga skeptilised, võivad nad rääkida absoluutsetest erinevustest."
Kuid isegi väikesed mõjud võivad aja jooksul muutuda oluliseks, eriti haiguse hilisemates staadiumides, kui lagunemine toimub kiiremini, ütleb Walsh. "Lõppkokkuvõttes sõltub see sellest, mida te arvate, milline on pikaajaline mõju, ja meil pole sellele vastust."
Mõned pikaajalised andmed on nüüd saadaval. Eelmisel kuul Philadelphias toimunud Alzheimeri assotsiatsiooni rahvusvahelisel konverentsil (AAIC) esitlesid Eisai ja Biogen avatud jätkuuuringu tulemusi, mis jätkasid lekanemabi saanud patsientide jälgimist pärast III faasi uuringu lõpetamist. Pärast kolmeaastast pidevat ravi paranes enam kui pooltel patsientidest ja enamik ARIA juhtudest tekkis ravi esimese kuue kuu jooksul. Samuti teatasid nad, et kognitiivse languse määr taastus platseebo tasemele, kui inimesed lõpetasid ravimi võtmise, isegi kui amüloidnaastud olid eemaldatud enne ravi lõpetamist.
Mõned on nende tulemuste suhtes optimistlikud – Haassi sõnul on põnev näha, et ravim mitte ainult ei kõrvalda amüloidi, vaid aeglustab ka tau levikut, teise valgu, mis ladestub Alzheimeri tõvega inimeste ajudes tükkideks. Teised on ettevaatlikumad. Londoni Imperial College'i neuroloog Paresh Malhotra juhib tähelepanu, et AAIC-l esitatud positiivseid tulemusi ei võrreldud platseeboga, mistõttu on ravimi pikaajalise efektiivsuse määramiseks vaja rohkem andmeid.
Mure teeb ka kulu. Walsh ütleb, et arvestades ravimi tagasihoidlikku mõju, on raske põhjendada ravimi manustamiskulusid (mis maksab USA-s üle 20 000 dollari aastas) ja vajalikke protseduure, nagu pildistamine ja geenitestid, et tuvastada selle saamiseks sobivaid inimesi.
Ohutusprobleemid
Suurim mure lekanemabiga on ARIA, mille eest hoiatas USA toidu- ja ravimiamet (FDA) heakskiitmisel. Kuigi enamik juhtumeid on asümptomaatilised – ja esialgses 18-kuulises kliinilises uuringus ei teatatud ühestki –, esines uuringu pikendatud faasis mõningaid ARIA-ga seotud surmajuhtumeid.
Mõned eksperdid ütlevad, et kuigi raske ARIA risk on madal, on oluline arvestada ka sellega, et ravimit manustatakse Alzheimeri tõve varases staadiumis. "See on periood, mil inimestel on kõige rohkem kaotada," ütleb Schrag. "Selle akna ajal julgustame patsiente sageli reisima, mõtlema oma bucket listile ja saavutama asju, mida nad tahavad elus saavutada."
Hollandi Leideni ülikooli meditsiinikeskuse neuroloog Ellis van Etten ütleb, et ARIA kohta on veel palju vastamata küsimusi ja seda, kuidas arstid peaksid reageerima, kui nad näevad, et patsientidel tekivad ravi ajal need kõrvalekalded. Näiteks: Kellel tekib tõsine või eluohtlik ARIA? Millal muutub ARIA kahjutuks kahjulikuks ja millal tuleks ravi lekanemabiga lõpetada?
Paljud samad küsimused kasu ja riskide kohta kehtivad ka teise amüloidi puhastava antikeha, donanemabi kohta, mille valmistas Eli Lilly Indianapolises, Indiana ja mille FDA kiitis juulis heaks. Donanemab näib vähendavat kognitiivset langust ligikaudu sama palju kui lekanamab – ja seda on seostatud ARIA-ga seotud surmajuhtumitega.
"Me teame biomarkerite tööst, et need antikehad puhastavad amüloidi, seega teame, et need käsitlevad haiguse põhimehhanismi," ütleb Malhotra. Kuid nendest ravimitest üksi tõenäoliselt ei piisa ja oluline on käsitleda ka haiguse muid aspekte. "On väga tõenäoline, et 10 aasta pärast räägime kombineeritud ravist ja amüloidi kliirens on selle lähenemisviisi osa."

 Suche
Suche
 Mein Konto
Mein Konto