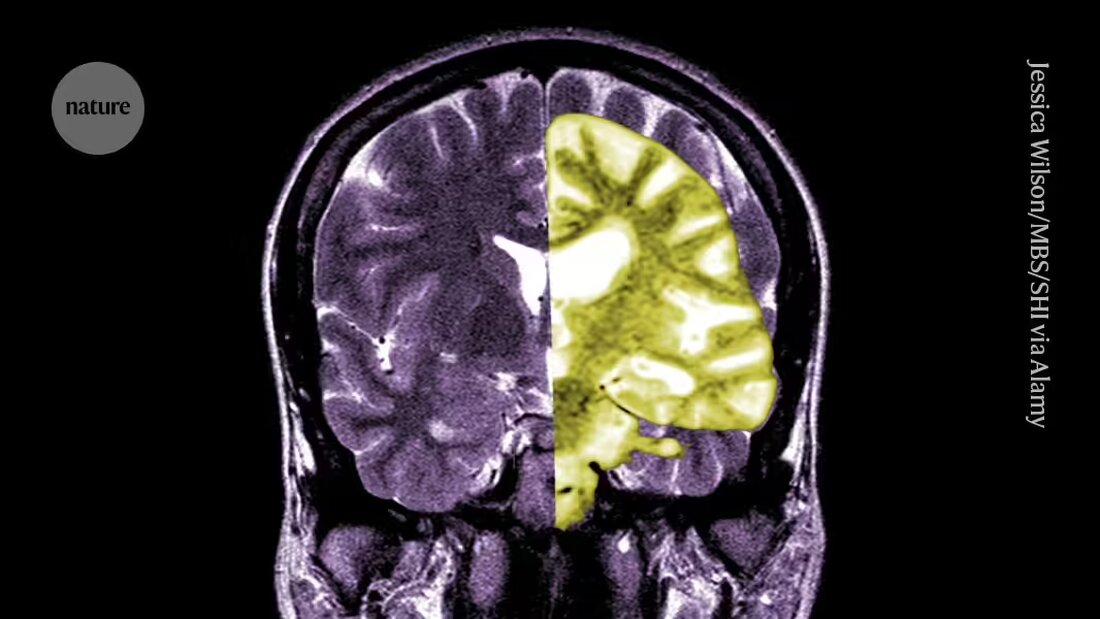
Η συζήτηση για το φάρμακο Alzheimer lecanemab - ένα από τα πρώτα φάρμακα που επιβραδύνει τη γνωστική πτώση στους ανθρώπους - εντείνεται μεταξύ των ερευνητών και των κλινικών ιατρών για το εάν τα πιθανά οφέλη της θεραπείας υπερτερούν των κινδύνων της.
Στις 22 Αυγούστου, η Ρυθμιστική Υπηρεσία Φαρμάκων και Προϊόντων Υγείας της Βρετανίας έδωσε το πράσινο φως στο φάρμακο. Ταυτόχρονα, ωστόσο, η βρετανική ρυθμιστική αρχή υγείας NICE, η οποία καθορίζει εάν προσφέρονται φάρμακα σε ασθενείς στην κρατικά χρηματοδοτούμενη Εθνική Υπηρεσία Υγείας της Βρετανίας (NHS), δήλωσε σε προσχέδιο ότι το lecanemab δεν θα διατίθεται στο NHS επειδή τα οφέλη ήταν πολύ μικρά για να δικαιολογήσουν το υψηλό κόστος.
«Ο ασυνήθιστα μεγάλος χρόνος που ξόδεψαν για την αναθεώρηση του φαρμάκου υποδηλώνει ότι αυτή δεν ήταν μια εύκολη ή απλή απόφαση», δήλωσε ο ψυχίατρος Ρόμπερτ Χάουαρντ του University College του Λονδίνου σε δήλωση στο Science Media Center στη Βρετανία.
Οι ρυθμιστικές αρχές των ΗΠΑ ήταν οι πρώτοι που ενέκριναν το φάρμακο το 2023 και ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) επανεξετάζει τώρα την απόφασή του μετά από προσφυγή της φαρμακευτικής εταιρείας.
Στόχος αμυλοειδούς
Η απόφαση του EMA έλαβε επίσης ανάμικτες αντιδράσεις από την κοινότητα του Αλτσχάιμερ. «Τα συναισθήματα είναι πραγματικά έντονα εδώ», λέει ο βιοχημικός Christian Haass του Πανεπιστημίου Ludwig Maximilians στο Μόναχο της Γερμανίας, ο οποίος διαφωνεί με την απόφαση. «Είναι το πρώτο φάρμακο τροποποίησης της νόσου που είχαμε σε περισσότερα από 30 χρόνια». Η άρνηση πρόσβασης των ασθενών στο lecanemab σημαίνει ότι πολλοί χάνουν την ευκαιρία να κερδίσουν πολύτιμο χρόνο, σύμφωνα με τον Haass.
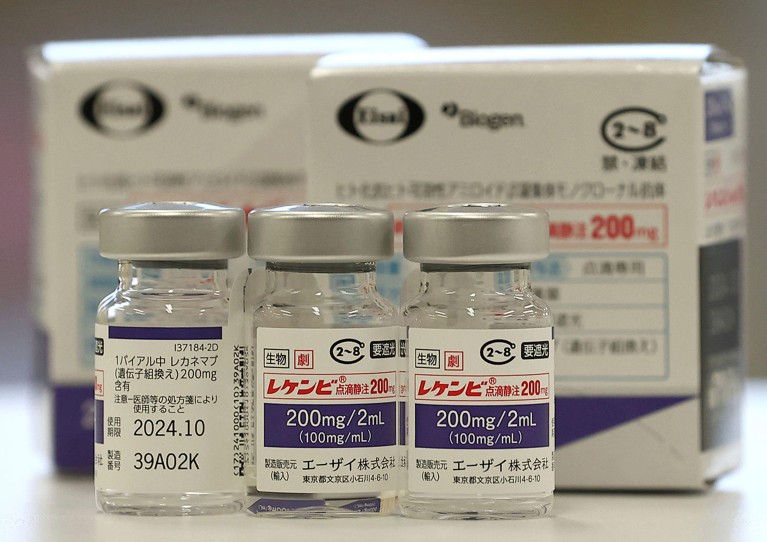
Το Lecanemab, ή Leqembi, είναι ένα μονοκλωνικό αντίσωμα που εξαλείφει το αμυλοειδές, μια ουσία που συσσωρεύεται σε τοξικές συστάδες στον εγκέφαλο ατόμων με Αλτσχάιμερ. Το φάρμακο, που παρασκευάζεται από την Eisai στο Τόκιο και τη Biogen στο Κέιμπριτζ της Μασαχουσέτης, είναι επίσης εγκεκριμένο στην Κίνα, την Ιαπωνία, τη Νότια Κορέα και τα Ηνωμένα Αραβικά Εμιράτα.
Άλλοι επικροτούν τον EMA, λέγοντας ότι ενώ το φάρμακο ήταν αποτελεσματικό στη μείωση των επιπέδων αμυλοειδούς στον εγκέφαλο, παραμένει ασαφές εάν η προκύπτουσα μείωση της γνωστικής έκπτωσης θα οδηγήσει σε κλινικά σχετικά οφέλη για τους ασθενείς. Δηλώνουν ότι η πιθανότητα σοβαρών επιπλοκών όπως αιμορραγία ή πρήξιμο στον εγκέφαλο που προκαλείται από μια παρενέργεια που ονομάζεται επιδράσεις απεικόνισης που σχετίζονται με το αμυλοειδές (ARIA), αν και μικρή, είναι μια σημαντική ανησυχία. «Μια λογική εκτίμηση των κινδύνων έναντι των οφελών αυτού του φαρμάκου θα πρέπει να κάνει τους ανθρώπους να είναι πολύ δύσπιστοι», λέει ο Μάθιου Σραγκ, νευρολόγος στο Πανεπιστήμιο Vanderbilt στο Νάσβιλ του Τενεσί.
Μέτρια εφέ
Το εάν η lecanemab χορηγούμενη με έγχυση παρέχει στους ανθρώπους κλινικά σημαντικές μειώσεις στη γνωστική έκπτωση έχει συζητηθεί εδώ και καιρό.
Μια κλινική δοκιμή Φάσης ΙΙΙ του φαρμάκου, που δημοσιεύθηκε το 2022, περιελάμβανε 1.795 άτομα στα πρώιμα στάδια της νόσου του Αλτσχάιμερ και διαπίστωσε ότι όσοι έλαβαν το φάρμακο παρουσίασαν μείωση 27% στη γνωστική έκπτωση μετά από 18 μήνες σε σύγκριση με όσους έλαβαν εικονικό φάρμακο. Ορισμένοι ερευνητές γιόρτασαν την είδηση ως νίκη για το πεδίο. Ωστόσο, άλλοι υποστήριξαν ότι τα αποτελέσματα είναι πολύ μικρά για να έχουν σημαντική επίδραση στους ασθενείς.
Ένας από τους λόγους αυτής της διαφοράς στην οπτική γωνία είναι ο τρόπος με τον οποίο οι άνθρωποι βλέπουν τα δεδομένα, λέει ο Sebastian Walsh, ερευνητής δημόσιας υγείας στο Πανεπιστήμιο του Cambridge, στο Ηνωμένο Βασίλειο. Η μείωση κατά 27% αντιπροσωπεύει τη σχετική διαφορά στην ποσότητα της γνωστικής έκπτωσης που βίωσε η ομάδα φαρμάκων σε σύγκριση με την ομάδα του εικονικού φαρμάκου. Ωστόσο, η απόλυτη διαφορά στη γνωστική λειτουργία είναι πολύ μικρότερη: 0,45 μονάδες σε μια κλίμακα 18 βαθμών. «Οι άνθρωποι μπορούν να εξαγάγουν ό,τι θέλουν από το μέγεθος του εφέ», λέει ο Walsh. «Αν θέλουν να πουλήσουν το φάρμακο, θα μπορούσαν να επικεντρωθούν σε σχετικές αλλαγές – και αν είναι πολύ δύσπιστοι, θα μπορούσαν να μιλήσουν για τις απόλυτες διαφορές».
Αλλά ακόμη και μικρές επιδράσεις μπορεί να γίνουν σημαντικές με την πάροδο του χρόνου, ιδιαίτερα στα τελευταία στάδια της νόσου όταν η υποβάθμιση συμβαίνει πιο γρήγορα, λέει ο Walsh. «Σε τελική ανάλυση εξαρτάται από το τι πιστεύετε ποιος θα είναι ο μακροπρόθεσμος αντίκτυπος και δεν έχουμε απάντηση σε αυτό».
Ορισμένα μακροπρόθεσμα δεδομένα είναι πλέον διαθέσιμα. Στο Διεθνές Συνέδριο της Ένωσης Alzheimer (AAIC) στη Φιλαδέλφεια τον περασμένο μήνα, οι Eisai και Biogen παρουσίασαν αποτελέσματα από μια ανοιχτή μελέτη επέκτασης που συνέχισε να παρακολουθεί ασθενείς που έλαβαν lecanemab μετά την ολοκλήρωση της δοκιμής Φάσης III. Μετά από τρία χρόνια συνεχούς θεραπείας, περισσότεροι από τους μισούς ασθενείς παρουσίασαν βελτίωση και οι περισσότερες περιπτώσεις ARIA εμφανίστηκαν τους πρώτους έξι μήνες της θεραπείας. Ανέφεραν επίσης ότι ο ρυθμός γνωστικής έκπτωσης επέστρεψε στα επίπεδα εικονικού φαρμάκου όταν οι άνθρωποι σταμάτησαν να παίρνουν το φάρμακο, ακόμη και αν οι πλάκες αμυλοειδούς είχαν αφαιρεθεί πριν τη διακοπή της θεραπείας.
Μερικοί είναι αισιόδοξοι για αυτά τα αποτελέσματα - ο Haass λέει ότι είναι συναρπαστικό να βλέπεις ότι το φάρμακο όχι μόνο εξαλείφει το αμυλοειδές, αλλά και επιβραδύνει την εξάπλωση του tau, μιας άλλης πρωτεΐνης που συσσωρεύεται σε συστάδες στον εγκέφαλο ατόμων με Αλτσχάιμερ. Άλλοι είναι πιο προσεκτικοί. Ο Paresh Malhotra, νευρολόγος στο Imperial College του Λονδίνου, επισημαίνει ότι τα θετικά αποτελέσματα που παρουσιάστηκαν στο AAIC δεν συγκρίθηκαν με ένα εικονικό φάρμακο, επομένως χρειάζονται περισσότερα δεδομένα για να προσδιοριστεί η μακροπρόθεσμη αποτελεσματικότητα του φαρμάκου.
Το κόστος είναι επίσης ανησυχητικό. Ο Walsh λέει ότι δεδομένων των μέτριων επιδράσεων του φαρμάκου, είναι δύσκολο να δικαιολογηθεί το κόστος χορήγησης του φαρμάκου (το οποίο κοστίζει περισσότερα από 20.000 $ ετησίως στις ΗΠΑ) και οι διαδικασίες που απαιτούνται, όπως απεικόνιση και γενετικός έλεγχος, για τον εντοπισμό των κατάλληλων ατόμων για να το λάβουν.
Ανησυχίες για την ασφάλεια
Η μεγαλύτερη ανησυχία για το lecanemab είναι το ARIA, για το οποίο προειδοποίησε στην έγκρισή του η Υπηρεσία Τροφίμων και Φαρμάκων των ΗΠΑ (FDA). Αν και οι περισσότερες περιπτώσεις είναι ασυμπτωματικές - και καμία δεν αναφέρθηκε κατά την αρχική κλινική δοκιμή διάρκειας 18 μηνών - υπήρξαν ορισμένοι θάνατοι που σχετίζονται με το ARIA στην εκτεταμένη φάση της μελέτης.
Ορισμένοι ειδικοί λένε ότι αν και ο κίνδυνος σοβαρής ARIA είναι χαμηλός, είναι επίσης σημαντικό να ληφθεί υπόψη ότι το φάρμακο χορηγείται στα πρώτα στάδια της νόσου Αλτσχάιμερ. «Αυτή είναι η περίοδος κατά την οποία οι άνθρωποι έχουν τα περισσότερα να χάσουν», λέει ο Schrag. «Κατά τη διάρκεια αυτού του παραθύρου, συχνά ενθαρρύνουμε τους ασθενείς να ταξιδέψουν, να σκεφτούν τη λίστα τους και να πραγματοποιήσουν τα πράγματα που θέλουν να πετύχουν στη ζωή τους».
Ο Έλις βαν Έτεν, νευρολόγος στο Ιατρικό Κέντρο του Πανεπιστημίου του Λέιντεν στην Ολλανδία, λέει ότι υπάρχουν ακόμα πολλά αναπάντητα ερωτήματα σχετικά με το ARIA και πώς πρέπει να ανταποκρίνονται οι γιατροί όταν βλέπουν ασθενείς να αναπτύσσουν αυτές τις ανωμαλίες κατά τη διάρκεια της θεραπείας. Για παράδειγμα: Ποιος θα αναπτύξει σοβαρή ή απειλητική για τη ζωή ARIA; Σε ποιο σημείο το ARIA μετατρέπεται από αβλαβές σε επιβλαβές και πότε πρέπει να σταματήσει η θεραπεία με lecanemab;
Πολλές από τις ίδιες ερωτήσεις σχετικά με τα οφέλη και τους κινδύνους ισχύουν επίσης για ένα άλλο αντίσωμα καθαρισμού του αμυλοειδούς, το donanemab — που παρασκευάστηκε από την Eli Lilly στην Ινδιανάπολη της Ιντιάνα — το οποίο εγκρίθηκε από τον FDA τον Ιούλιο. Το Donanemab φαίνεται να παρέχει περίπου την ίδια μείωση στη γνωστική έκπτωση με το lecanamab – και έχει συνδεθεί με θανάτους που σχετίζονται με το ARIA.
«Γνωρίζουμε από την εργασία βιοδεικτών ότι αυτά τα αντισώματα καθαρίζουν το αμυλοειδές, επομένως γνωρίζουμε ότι αντιμετωπίζουν έναν θεμελιώδη μηχανισμό της νόσου», λέει ο Malhotra. Αλλά αυτά τα φάρμακα από μόνα τους πιθανώς δεν θα είναι αρκετά και θα είναι σημαντικό να αντιμετωπιστούν και άλλες πτυχές της νόσου. «Είναι πολύ πιθανό σε 10 χρόνια να μιλάμε για συνδυαστικές θεραπείες και ότι η κάθαρση αμυλοειδούς θα είναι μέρος αυτής της προσέγγισης».

 Suche
Suche
 Mein Konto
Mein Konto